题目内容
某烃类化合物A的用仪器可以测出其相对分子质量为84,分子中含有碳碳双键,分子中只有一种类型的氢.
(1)现有以下的实验室仪器:
A.1H核磁共振仪 B.质谱仪 C.红外光谱仪 D.元素分析仪
请你选择分别用什么仪器.①测出相对分子质量 (填字母代号,下同)、
②测出官能团碳碳双键 、③测出几种类型的氢 .
(2)结合题给信息,可以判断A的结构简式为 ;
A中的碳原子是以什么形式杂化? ;
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体.

反应②的化学方程式为 ;
C的名称为 ;反应类型为 ;.
E2的结构简式是 ;④、⑤的反应类型依次是 、 .
(1)现有以下的实验室仪器:
A.1H核磁共振仪 B.质谱仪 C.红外光谱仪 D.元素分析仪
请你选择分别用什么仪器.①测出相对分子质量
②测出官能团碳碳双键
(2)结合题给信息,可以判断A的结构简式为
A中的碳原子是以什么形式杂化?
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体.

反应②的化学方程式为
C的名称为
E2的结构简式是
考点:有机物实验式和分子式的确定,有机物的推断
专题:有机物的化学性质及推断
分析:(1)1H核磁共振仪用于测定氢原子种类;质谱仪用于测定有机物的相对分子质量;红外光谱仪用于测定有机物的中化学键的类型;元素分析仪用于测定有机物中元素的种类;
(2)A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,则A应为烯烃,设分子式为CnH2n,则有14n=84,n=6,根据核磁共振氢谱表明分子中只有一种类型的氢,写出结构简式;根据价层电子对互斥理论来分析解答,4个σ键且不含孤电子对采用sp3杂化,含有3个σ键且不含孤电子对采用sp2杂化;
(3)(CH3)2C=C(CH3)2与液溴反应生成B,B为:(CH3)2C(Br)C(Br)(CH3)2,B在氢氧化钠、乙醇作用下加热,发生消去反应生成C,C为CH2=C(CH3)-C(CH3)=CH2,C与溴发生1,2-加成生成D1,故D1为CH2BrCBr(CH3)-C(CH3)=CH2,D1在氢氧化钠水溶液中发生水解反应生成E1,E1为HOCH2C=CCH2OH,D1、D2互为同分异构体,故反应④发生1,4-加成,D2为CH2BrC(CH3)=C(CH3)CH2Br,D2在氢氧化钠水溶液中发生水解反应生成E2,E2为HOCH2C(CH3)=C(CH3)CH2OH,据此解答.
(2)A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,则A应为烯烃,设分子式为CnH2n,则有14n=84,n=6,根据核磁共振氢谱表明分子中只有一种类型的氢,写出结构简式;根据价层电子对互斥理论来分析解答,4个σ键且不含孤电子对采用sp3杂化,含有3个σ键且不含孤电子对采用sp2杂化;
(3)(CH3)2C=C(CH3)2与液溴反应生成B,B为:(CH3)2C(Br)C(Br)(CH3)2,B在氢氧化钠、乙醇作用下加热,发生消去反应生成C,C为CH2=C(CH3)-C(CH3)=CH2,C与溴发生1,2-加成生成D1,故D1为CH2BrCBr(CH3)-C(CH3)=CH2,D1在氢氧化钠水溶液中发生水解反应生成E1,E1为HOCH2C=CCH2OH,D1、D2互为同分异构体,故反应④发生1,4-加成,D2为CH2BrC(CH3)=C(CH3)CH2Br,D2在氢氧化钠水溶液中发生水解反应生成E2,E2为HOCH2C(CH3)=C(CH3)CH2OH,据此解答.
解答:
解:(1)①测出相对分子质量质谱仪;②测出官能团碳碳双键红外光谱仪;③测出几种类型的氢1H核磁共振仪,故选:B;C;A;
(2)A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,则A应为烯烃,设分子式为CnH2n,则有14n=84,n=6,又因为核磁共振氢谱表明分子中只有一种类型的氢,其结构简式应为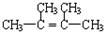 ;在
;在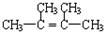 分子中,双键碳原子含有3个σ键且不含孤电子对,所以采用sp2杂化,甲基碳原子含有4个σ键且不含孤电子对,所以采用sp3杂化,
分子中,双键碳原子含有3个σ键且不含孤电子对,所以采用sp2杂化,甲基碳原子含有4个σ键且不含孤电子对,所以采用sp3杂化,
故答案为: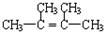 ;sp2和sp3;
;sp2和sp3;
(3)反应②是B为:(CH3)2C(Br)C(Br)(CH3)2在氢氧化钠醇溶液、加热条件下发生消去反应,生成CH2=C(CH3)-C(CH3)=CH2,该反应的化学方程式为: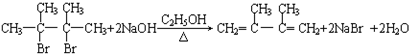 C为CH2=C(CH3)-C(CH3)=CH2,的化学名称是2,3-二甲基-1,3-丁二烯,由上述分析可知,E2的结构简式是:HOCH2C(CH3)=C(CH3)CH2OH,
C为CH2=C(CH3)-C(CH3)=CH2,的化学名称是2,3-二甲基-1,3-丁二烯,由上述分析可知,E2的结构简式是:HOCH2C(CH3)=C(CH3)CH2OH,
反应④是1,4-加成反应、反应⑥是取代反应,
故答案为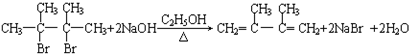 ;2,3-二甲基-1,3-丁二烯;消去反应;HOCH2C(CH3)=C(CH3)CH2OH;1,4-加成反应;取代反应.
;2,3-二甲基-1,3-丁二烯;消去反应;HOCH2C(CH3)=C(CH3)CH2OH;1,4-加成反应;取代反应.
(2)A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,则A应为烯烃,设分子式为CnH2n,则有14n=84,n=6,又因为核磁共振氢谱表明分子中只有一种类型的氢,其结构简式应为
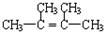 ;在
;在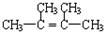 分子中,双键碳原子含有3个σ键且不含孤电子对,所以采用sp2杂化,甲基碳原子含有4个σ键且不含孤电子对,所以采用sp3杂化,
分子中,双键碳原子含有3个σ键且不含孤电子对,所以采用sp2杂化,甲基碳原子含有4个σ键且不含孤电子对,所以采用sp3杂化,故答案为:
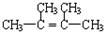 ;sp2和sp3;
;sp2和sp3;(3)反应②是B为:(CH3)2C(Br)C(Br)(CH3)2在氢氧化钠醇溶液、加热条件下发生消去反应,生成CH2=C(CH3)-C(CH3)=CH2,该反应的化学方程式为:
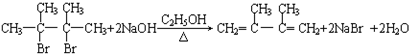 C为CH2=C(CH3)-C(CH3)=CH2,的化学名称是2,3-二甲基-1,3-丁二烯,由上述分析可知,E2的结构简式是:HOCH2C(CH3)=C(CH3)CH2OH,
C为CH2=C(CH3)-C(CH3)=CH2,的化学名称是2,3-二甲基-1,3-丁二烯,由上述分析可知,E2的结构简式是:HOCH2C(CH3)=C(CH3)CH2OH,反应④是1,4-加成反应、反应⑥是取代反应,
故答案为
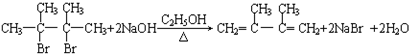 ;2,3-二甲基-1,3-丁二烯;消去反应;HOCH2C(CH3)=C(CH3)CH2OH;1,4-加成反应;取代反应.
;2,3-二甲基-1,3-丁二烯;消去反应;HOCH2C(CH3)=C(CH3)CH2OH;1,4-加成反应;取代反应.
点评:本题考查有机物推断,涉及卤代烃、烯、醇等的性质以及分子式的求解、同分异构体、有机化学反应类型和方程式的书写等,题目综合性较大,注意二烯烃的加成反应,难度中等.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列过程要吸收热量的是( )
| A、甲烷在空气中燃烧 |
| B、碳酸钙受热分解 |
| C、镁条溶于盐酸 |
| D、浓硫酸溶于水 |





 与BrMgCH2(CH2)3CH2MgBr在一定条件下发生类似反应①的反应,生成的有机化合物Ⅵ(分子式为C16H17N)的结构简式为
与BrMgCH2(CH2)3CH2MgBr在一定条件下发生类似反应①的反应,生成的有机化合物Ⅵ(分子式为C16H17N)的结构简式为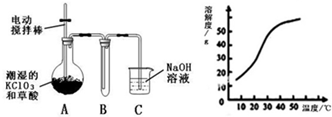 Ⅰ.二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.
Ⅰ.二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.