题目内容
17.下列关于硅单质及其化合物的说法正确的是( )①硅是构成一些岩石和矿物的基本元素 ②水泥、玻璃、水晶饰物都是硅酸盐制品 ③硅酸盐Na2Fe2Si3O10用氧化物的形式表示为:Na2O•2FeO•3SiO2 ④陶瓷是人类应用很早的硅酸盐材料.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
分析 ①几乎所有的岩石和矿物都含有硅酸盐或者二氧化硅;
②水晶主要成分是二氧化硅,属于氧化物;
③硅酸盐改写为氧化物形式:金属氧化物在前(活泼金属氧化物→较活泼金属氧化物),非金属氧化物在后,若同一元素有变价,那么低价在前,高价在后,H2O一般写在最后;
④陶瓷的主要原料是黏土,则陶瓷是人类应用很早的硅酸盐材料.
解答 解:①几乎所有的岩石和矿物都含有硅酸盐或者二氧化硅,所以硅是构成一些岩石和矿物的基本元素,故正确;
②水晶主要成分是二氧化硅,属于氧化物,不是硅酸盐,故错误;
③硅酸盐Na2Fe2Si3O10用氧化物的形式表示为:Na2O•Fe2O3•3SiO2,故错误;
④陶瓷的主要原料是黏土,则陶瓷是人类应用很早的硅酸盐材料,故正确;
故选:C.
点评 本题考查了硅及其化合物的用途,明确硅、二氧化硅、硅酸盐的性质是解题关键,注意对基础知识的积累.

练习册系列答案
相关题目
7.下列涉及有机物的说法正确的是( )
| A. | 甲烷和乙烷互为同分异构体 | |
| B. | 乙烯可以使溴水和酸性高锰酸钾溶液褪色,这些反应都属于氧化反应 | |
| C. | 乙醇和乙酸在常温下可直接反应生成乙酸乙酯,该反应属于加成反应 | |
| D. | 纤维素、蔗糖和淀粉酶在一定条件下都可发生水解反应 |
8.实验室制Cl2的反应如下:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,下列有关该反应的说法正确的是( )
| A. | MnO2是还原剂 | B. | HCl被还原 | ||
| C. | MnO2发生氧化反应 | D. | 每反应4molHCl转移2mol电子 |
5.现有C2H2、CH3CHO、乙二醇三种蒸汽的混合物,已知含碳量为a%,则氢的含量为( )
| A. | $\frac{a}{12}$% | B. | $\frac{a}{27}$% | C. | $\frac{1}{9}-\frac{a}{27}$% | D. | 无法计算 |
12.一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL 4.40mol/L盐酸中,充分反应后产生896mL H2(标准状况),残留固体1.28g.过滤,滤液中无Cu2+.将滤液加水稀释到200mL,测得其中c(H+)为0.400mol/L.下列判断正确的是( )
| A. | 残留固体中一定不含有铁 | B. | 滤液中可能含有Fe3+ | ||
| C. | 原混合物中n(Fe)>n(Fe2O3)+n(CuO) | D. | 原混合物中铁为3.36 g |
2.下列说法错误的是( )
| A. | 用酸性KMnO4溶液鉴别CH3CH3和CH2=CH2 | |
| B. | 将盛有等体积CH4和Cl2的大试管倒扣在水槽中光照,试管内不能充满液体 | |
| C. | 用NaOH溶液除去乙酸乙酯中的少量乙酸 | |
| D. | 用NaOH溶液和新制Cu(OH)2悬浊液检验淀粉在稀H2SO4作用下是否水解 |
9.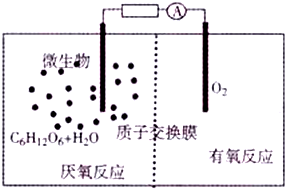 微生物电池是指在微生物的作用下将化学能转化为电能的装置(总反应方程式为C6H12O6+6O2═6CO2+6H2O),其工作原理如图所示.下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置(总反应方程式为C6H12O6+6O2═6CO2+6H2O),其工作原理如图所示.下列有关微生物电池的说法错误的是( )
 微生物电池是指在微生物的作用下将化学能转化为电能的装置(总反应方程式为C6H12O6+6O2═6CO2+6H2O),其工作原理如图所示.下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置(总反应方程式为C6H12O6+6O2═6CO2+6H2O),其工作原理如图所示.下列有关微生物电池的说法错误的是( )| A. | 正极区溶液的pH减小 | |
| B. | 微生物促进了反应中电子的转移 | |
| C. | 质子通过交换膜从负极区移向正极区6H2O+C6H12O6-24e-═6CO2+24H+ |
6.被誉为“光纤之父”的华人科学家高锟“在光学通信领域光在光纤中传输方面取得了开创性成就”.目前应用最广泛的无机光导纤维的主要原料为二氧化硅,下列关于二氧化硅的说法正确的是( )
| A. | SiO2溶于水生成的H2SiO3的酸性弱于H2CO3 | |
| B. | SiO2是一种空间立体网状结构的晶体,熔点高、硬度大 | |
| C. | 在SiO2晶体中,每个硅原子周围结合2个氧原子 | |
| D. | SiO2是一种酸性氧化物,所以不和任何酸反应 |
7.下列关于溶液中离子的说法正确的是( )
| A. | 0.2mol•L-1的Na2CO3溶液中离子浓度关系:c (Na+)=2c (CO32-)+c (HCO3-)+c (H2CO3) | |
| B. | 0.01mol•L-1的NH4Cl和0.01mol•L-1的NH3•H2O等体积混合后,若测得溶液中c (Cl-)>c (NH4+),则溶液中有关微粒的浓度关系: c (Cl-)>c (NH3•H2O)>c (NH4+)>c (H+)>c (OH-) | |
| C. | 0.1mol的NaHS和0.1mol的NaHSO4混合溶于水,配制成1L溶液,则混合溶液中离子浓度关系为:c (Na+)-0.1mol•L-1=2c (S2-)+c (H2S)+c (HS-) | |
| D. | 0.1mol•L-1的NaHCO3溶液中离子浓度关系:c (OH-)=c (H+)+c (H2CO3)-c (CO32-) |