��Ŀ����
| ʵ�� | ʵ������ | ���� |
| A | 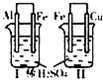 ���ձ��������������ݢ��ձ���ͭ���������� |
��ԣ�Al��Fe��Cu |
| B | 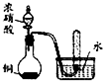 �Թ����ռ�����ɫ���� |
ͭ��Ũ����ķ�Ӧ������NO |
| C | 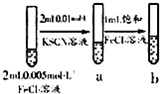 �Թ�b���Թ�a����Һ�ĺ�ɫ�� |
����Ӧ��Ũ�ȣ�ƽ��������Ӧ�����ƶ� |
| D | 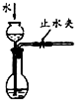 ����©����Һ�������ƿ��Һ���ұ��ֲ��� |
װ������������ |
| A��A | B��B | C��C | D��D |
B������ͭ��Ũ���ᷴӦ��ԭ���Լ�����������ˮ��Ӧ��ԭ�����н��
C��Fe��SCN��3ΪѪ��ɫ������Ӧ��Ũ�ȣ�������Һ��ɫ�仯�жϷ�Ӧ����
D�����ݼ��װ�������Ե�ԭ����ͨ���ı���ϵ��ѹǿʱ���������������ݵ����ɡ�ˮ�����γɡ�Һ��������ȣ����ж�װ�������Եĺû��������
B��Cu��Ũ���ᷴӦ����Ӧ�еĻ��ϼ۱仯Ϊ��HNO3��NԪ����+5�۽���ΪNO2��NԪ��+4�ۣ�HNO3����������NO2�ǻ�ԭ�������ʽΪ��Cu+4HNO3�TCu��NO3��2+2NO2��+2H2O�����ɵĺ���ɫ����������ˮ����������ԭ��Ӧ��3NO2+H2O=2HNO3+NO������ͼ���Թ����ռ�����ɫ����Ϊһ��������������ͭ��Ũ���ᷴӦ����һ����������B����
C��Fe3+��SCN-������ӦFe3++3SCN-?Fe��SCN��3��Fe��SCN��3ΪѪ��ɫ�������Ȼ�����Һ��Ũ�ȣ�������Һ��ɫ�仯���жϷ�Ӧ���������Һ��ɫ�����˵��ƽ��������Ӧ�����ƶ��������ܴﵽʵ��Ŀ�ģ���C��ȷ��
D����װ�õ������Լ�飬��Ҫ��ͨ������ѹǿ��������仯�����м��飬�н�ֹˮ�У���©���м�ˮ����Һ�������ƿ�ڵ�Һ�棬һ��ʱ���Һ��߶Ȳ����ޱ仯���仯˵��װ��©������֮��©������D��ȷ��
��ѡB��

 �������ͬ������ϵ�д�
�������ͬ������ϵ�д���������ʵ�����������Ľ��ͻ����õĽ��۴������
|
|
���������� |
���ͻ���� |
|
A |
��һС������ᴦ�������������ھƾ����ϼ��ȣ����ۻ��������䡣 |
������ܿ��γ��۵�����ߵ�����Ĥ������Ĥ��ס���ۻ����� |
|
B |
��һС�������Ͷ��ʢ����ˮ�Ҵ����Թ��У��ƿ����������ݡ� |
�Ҵ������к����ǻ� |
|
C |
��CaCl2��Һ�м������Na2SO4��Һ�����ú����ϲ���Һ�еμ�Na2CO3Ũ��Һ��������ɫ���ǡ� |
��ɫ����ΪCaCO3����ѧ��Ӧ���п����ԣ���ѧ��Ӧ�Ľ��̶���һ������ |
|
D |
��2 mL������Һ�м���ϡ���ᣬ����2 min����������Cu(OH)2�ڼ��ȣ����������� |
���������������²�ˮ�� |
��������ʵ�����������Ľ��ͻ����õĽ��۴������
| ���������� | ���ͻ���� | |
| A | ��һС������ᴦ�������������ھƾ����ϼ��ȣ����ۻ��������䡣 | ������ܿ��γ��۵�����ߵ�����Ĥ������Ĥ��ס���ۻ����� |
| B | ��һС�������Ͷ��ʢ����ˮ�Ҵ����Թ��У��ƿ����������ݡ� | �Ҵ������к����ǻ� |
| C | ��CaCl2��Һ�м������Na2SO4��Һ�����ú����ϲ���Һ�еμ�Na2CO3Ũ��Һ��������ɫ���ǡ� | ��ɫ����ΪCaCO3����ѧ��Ӧ���п����ԣ���ѧ��Ӧ�Ľ��̶���һ������ |
| D | ��2 mL������Һ�м���ϡ���ᣬ����2 min����������Cu(OH)2�ڼ��ȣ����������� | ���������������²�ˮ�� |
��������ʵ�����������Ľ��ͻ����õĽ��۴������
|
| ���������� | ���ͻ���� |
| A | ��һС������ᴦ�������������ھƾ����ϼ��ȣ����ۻ��������䡣 | ������ܿ��γ��۵�����ߵ�����Ĥ������Ĥ��ס���ۻ����� |
| B | ��һС�������Ͷ��ʢ����ˮ�Ҵ����Թ��У��ƿ����������ݡ� | �Ҵ������к����ǻ� |
| C | ��CaCl2��Һ�м������Na2SO4��Һ�����ú����ϲ���Һ�еμ�Na2CO3Ũ��Һ��������ɫ���ǡ� | ��ɫ����ΪCaCO3����ѧ��Ӧ���п����ԣ���ѧ��Ӧ�Ľ��̶���һ������ |
| D | ��2 mL������Һ�м���ϡ���ᣬ����2 min����������Cu(OH)2�ڼ��ȣ����������� | ���������������²�ˮ�� |
��������ʵ�����������Ľ��ͻ����õĽ��۴������
| | ���������� | ���ͻ���� |
| A | ��һС������ᴦ�������������ھƾ����ϼ��ȣ����ۻ��������䡣 | ������ܿ��γ��۵�����ߵ�����Ĥ������Ĥ��ס���ۻ����� |
| B | ��һС�������Ͷ��ʢ����ˮ�Ҵ����Թ��У��ƿ����������ݡ� | �Ҵ������к����ǻ� |
| C | ��CaCl2��Һ�м������Na2SO4��Һ�����ú����ϲ���Һ�еμ�Na2CO3Ũ��Һ��������ɫ���ǡ� | ��ɫ����ΪCaCO3����ѧ��Ӧ���п����ԣ���ѧ��Ӧ�Ľ��̶���һ������ |
| D | ��2 mL������Һ�м���ϡ���ᣬ����2 min����������Cu(OH)2�ڼ��ȣ����������� | ���������������²�ˮ�� |