��Ŀ����
�����12�֣�
������;�㷺�Ľ������ϣ�Ŀǰ��ҵ����Ҫ����������Ҫ�ɷֺ���������������������ȡ�����䳣���Ĺ������£�

��ش��������⣺
39������B����Ϊ������Ʒ���ۣ�����;Ϊ ����ҺC���������� ��
40������ʵ����ģ��������������IV��ԭ������ �н��У�ȷ���ù���ת����ȫ�ķ����ǶԲ�Ʒ�������������г����� ��
41��д���ٹ����з�����Ӧ�����ӷ���ʽ �����������У�NaOH��CO2��H2O�� ����ѭ��ʹ�á�
42����ʱ������õ�����ҺΪNa2CO3��NaHCO3�Ļ����Һ��ȡ��Ʒ��Һ50.00mL��ˮϡ�͵�1L������ȡ��20mL��������Һ������������Ƚ���ϴ�ӵ�ϴ��Һ����Ϊ�� ������Һ��������ķ����Ƕ��� ��Ӧ�Ŀ̶�ֵ��
43���ñ����ᣨ0.2000mol/L�����еζ���
��������ȡ20.00mL��Һ����̪��ָʾ�������ı�����12.00mL��
�ڴ�1Lϡ��Һ����ȡ10.00mL��������ָʾ�������ı�����15.00mL��
��50.00mLԭ��Ʒ��Һ��̼�����Ƶ�Ũ��Ϊ ��
44������III����ʱ��ΪʹD��Һ��ֻ��һ�����ʣ���ÿ����Һ���������ʯ�ҵ�����Ϊ ��
����12�֣�39.�������ɫ���� ��1��)�� AlO2����OH- (1�֣� OH����д���۷�)
40.������1�֣��ٽ������ա���ȴ��������ֱ���������γ����Ľ��������0.001g������к��ز�������1��)��
41.Al2O3+2OH��=2AlO2��+H2O (1�֣���ƽ����д����ѧʽ������)��CaO ��1��)
42.����ˮ������ˮ������Һ��1�֣������밼Һ����ʹ����У�1��)
43.1.2mol/L (2��) 44��201.6g(2��)
��������
���������39.������ĺ����������������������м���ǿ����Һ���ᷢ����Ӧ��Al2O3+ 2OH-= 2AlO2-+ H2O���������������ܽ⣬Ȼ����ˣ��õ�����ҺC�к���AlO2-������B�к���������������B����Ϊ������Ʒ���ۣ�����;Ϊ�������ɫ���ϣ���ҺC����������AlO2����OH-��
40.��Al(OH)3���գ������ֽⷴӦ����Al2O3��Ȼ�������ڵ�����������Al������������ʵ����ģ��������������IV��ԭ�����������н��У�ȷ���ù���ת����ȫ�ķ����ǶԲ�Ʒ�������������г�������ز��������ٽ������ա���ȴ��������ֱ���������γ����Ľ��������0.001g��
41.�ٹ����з�����Ӧ�����ӷ���ʽ��Al2O3+ 2OH-= 2AlO2-+ H2O�����������У�������CaCO3���ղ�����CaO��NaOH��CO2��H2O����ѭ��ʹ�á�
42����ʱ������õ�����ҺΪNa2CO3��NaHCO3�Ļ����Һ��ȡ��Ʒ��Һ50.00mL��ˮϡ�͵�1L������ȡ��20mL��������Һ������������Ƚ���ϴ�ӵ�ϴ��Һ����Ϊ����������ˮ���ζ���ϴ�Ӹɾ���Ϊ��ֹˮ����������Ӱ������Ũ�ȵIJⶨ����������ˮϴ�ӣ�Ϊʹ�γ�����Һ��ԭ�������ҺŨ����ͬ������ô���Һ��ϴ������Һ��������ķ���������Ҫƽ�ӣ������밼Һ����ʹ����ж�Ӧ�Ŀ̶�ֵ��
43���ñ����ᣨ0.2000mol/L�����еζ�����������ȡ20.00mL��Һ����̪��ָʾ�������ڷ�̪�ı�ɫ����8.1����ʱ�����ķ�Ӧ�ǣ�Na2CO3+ HCl=NaCl+ NaHCO3��n(Na2CO3)=n(HCl)= 0.2000mol/L��0.012L=2.4��10-3mol; ����ԭ50ml��Һ�к���Na2CO3�����ʵ�����n(Na2CO3)=2.4��10-3mol��(1000ml��20ml)=0.12mol;�ڴ�1Lϡ��Һ����ȡ10.00mL,�Լ�����ָʾ�������ڼ��ȵı�ɫ����4.4����ʱ�����ķ�ӦΪ��Na2CO3+ 2HCl=2NaCl+H2O+ CO2����NaHCO3+HCl=NaCl+H2O+ CO2�������ݢٿ�֪��10.00ml��Һ�к���Na2CO3�����ʵ�����1.2��10-3mol;����һ�����ı�����15.00mL������10.00ml��Һ�к���NaHCO3�����ʵ�����n(NaHCO3)= 0.2000mol/L��0.015L-2��1.2��10-3mol=1.2��10-3mol����ô��ԭ50ml��Һ�к���NaHCO3�����ʵ�����6��10-4mol��(1000ml��10ml)=0.06mol;��50.00mLԭ��Ʒ��Һ��̼�����Ƶ�Ũ��Ϊc(NaHCO3)=0.06mol��0.05L=1.2mol/L��
44����������Һ��������Һ��Na2CO3��NaHCO3�Ļ����Һ����50ml��Һ�к���n(Na2CO3)=0.12mol��n(NaHCO3)= 0.06mol,����1L��Һ�к��е����ʵ����ʵ����ǣ�n(Na2CO3)= 0.12mol��(1000ml��50ml)=2.4mol��n(NaHCO3)= 0.06mol��(1000ml��50ml)=1.2mol������в���III����ʱ��CaO��H2O������Ӧ����Ca(OH)2, Ca(OH)2��Na2CO3��NaHCO3������Ӧ����CaCO3��NaOH��ˮ��ΪʹD��Һ��ֻ��ֻ����NaOHһ�����ʣ������Ԫ���غ�ɵ�n(CaO)=n(CaCO3)= n(Na2CO3)+ n(NaHCO3)= 2.4mol+1.2mol=3.6mol������ÿ����Һ���������ʯ�ҵ�����Ϊm(CaO)= 3.6mol��56g/mol=201.6g��
���㣺����Al2O3�����ʡ�Fe2O3����;�������ķ��뷽�������ʺ����IJⶨ����Ӧ��ע�����������ʹ�á���Ӧ�����ӷ���ʽ����д�����ʵ�ѭ�����õ�֪ʶ��

��11�֣�����ʵ�ˮ��Һ�д��ڵ���ƽ�⡣
��1�������dz��������ᡣ
�ٴ�����ˮ��Һ�еĵ��뷽��ʽΪ_________��
�����з����У�����ʹ����ϡ��Һ��CH3COOH����̶��������__________������ĸ��ţ���
a���μ�����Ũ���� b������Һ
c����ˮϡ�� d���������������ƾ���
��2����0.1 mol��L-1NaOH��Һ�ֱ�ζ������Ϊ20.00 mL��Ũ�Ⱦ�Ϊ0.1mol��L-1������ʹ�����Һ���õ��ζ���������ҺpH�����NaOH��Һ������仯�������ζ����ߡ�
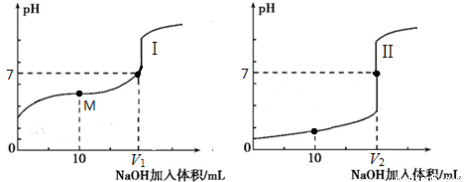
�ٵζ������������_____���I������
�ڵζ���ʼǰ��������Һ����ˮ�������c(H+)������_____��
��V1��V2�Ĺ�ϵ��V1_____V2���>������=����<������
��M���Ӧ����Һ�У������ӵ����ʵ���Ũ���ɴ�С��˳����_________��
��3��Ϊ���о������ܽ�ƽ��ͳ���ת����ijͬѧ�������ϲ��������ʵ�顣
���ϣ�AgSCN�ǰ�ɫ��������ͬ�¶��£��ܽ�ȣ�AgSCN > AgI��
�������� | ���� |
����1����2 mL 0.005 mol��L-1 AgNO3��Һ�м���2 mL 0.005 mol��L-1 KSCN��Һ�����á� | ���ְ�ɫ������ |
����2��ȡ1 mL�ϲ���Һ���Թ��У��μ�1��2mol��L-1 Fe(NO3)3��Һ�� | ��Һ���ɫ�� |
����3������2����Һ�У���������5��3 mol��L-1 AgNO3��Һ�� | ����a����Һ��ɫ��dz�� |
����4������1���µ���Һ�м���5��3 mol��L-1 KI��Һ�� | ���ֻ�ɫ������ |
��д������2����Һ���ɫ�����ӷ���ʽ__________________��
�ڲ���3������a��_____________________��
���û�ѧƽ��ԭ�����Ͳ���4��ʵ������______________________��
(15�֣�������ʯ����Ҫ�ɷ�ΪFeS2������FeS���������������в���Fe��SԪ�أ��Ҹ����²�������ѧ�仯�������ҹ���������᳧��ȡ�������Ҫԭ�ϡ�ij��ѧ��ȤС��Ըû�����ʯ��������ʵ��̽������m 1 g�û�����ʯ����Ʒ������ͼװ�ã��гֺͼ���װ���ԣ���ʯӢ���У���a�����ϵػ���ͨ��������������ջ�������Ʒ����Ӧ��ȫ��

�䷴Ӧ�Ļ�ѧ����ʽΪ��4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
4FeS + 7O2 2Fe2O3+4SO2
2Fe2O3+4SO2
��ʵ��һ���ⶨ��Ԫ�صĺ���
��Ӧ��������ƿ�е���Һ�������´�����

��1�����������������________________________________________________________��
��2����Ӧ��������ƿ�е���Һ�������H2O2��Һ��Ŀ���ǣ��û�ѧ����ʽ��ʾ��_________��H2O2���Կ�����һ�ֺ������ᣬд������뷽��ʽ�� ��
��3���û�����ʯ����Ԫ�ص���������Ϊ ���г�����ʽ���ɣ���
��ʵ������ⶨ��Ԫ�صĺ���

��4�����У�������������ԭ����������õ���Ԫ�صĺ���_______���ƫ����ƫС������Ӱ�족����
��5�����У���Ҫ�õ����������ձ�������������ͷ�ι��⣬����_________________��
��6��ijͬѧһ���������Ĵεζ�ʵ�飬ʵ������¼���£�
ʵ����� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
����KMnO4��Һ���/mL | 25.00 | 25.03 | 20.00 | 24.97 |
�����������ݣ������ϡ��Һ��Fe2+�����ʵ���Ũ��Ϊc(Fe2+) ��_______________��
��֪��H2(g) + Br2(g) �� 2HBr(g) ��H= ��72 kJ/mol��1mol Br2(g)Һ���ų�������Ϊ30 kJ����������������±��������������е�aֵΪ
һ��״̬�ķ��� | H2(g) | Br2(l) | HBr(g) |
1 mol�÷����еĻ�ѧ���������յ�����/kJ | 436 | a | 369 |
A��404 B��344 C��260 D��200



 R��Mg X�������Լ�����
R��Mg X�������Լ�����