题目内容
16.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )| A. | 常温常压下,Cu-Zn原电池中,正极产生1.12LH2时,转移的电子数应小于0.1NA | |
| B. | 1molSO2与足量O2在一定条件下反应生成SO2,共转移2NA个电子 | |
| C. | 2.1gDTO中所含中子数为NA | |
| D. | 常温常压下,28gC2H4、CO的混合气体中含有碳原子的数目为1.5NA |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、二氧化硫和氧气的反应为可逆反应;
C、DTO的摩尔质量为21g/mol;
D、C2H4、CO的摩尔质量均为28g/mol,但乙烯中含2个碳原子,CO中含一个碳原子.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故正极产生的氢气的物质的量小于0.05mol,则转移电子数小于0.1NA个,故A正确;
B、二氧化硫和氧气的反应为可逆反应,故不能进行彻底,则转移的电子数小于2NA个,故B错误;
C、DTO的摩尔质量为21g/mol,故2.1gDTO的物质的量为0.1mol,而DTO中含11个中子,故0.1molDTO中含1.1NA个中子,故C错误;
D、C2H4、CO的摩尔质量均为28g/mol,故28g混合物的物质的量为1mol,但乙烯中含2个碳原子,CO中含一个碳原子,且两者比例不确定,故1mo混合物中含有的碳原子的个数不确定,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
11.常温下,下列有关说法正确的是( )
| A. | 0.1 mol•L-1的Na2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| B. | pH=11的氨水与pH=3的硫酸各1L混合后,c(NH4+)>2c(SO42-) | |
| C. | pH=11的氨水与pH=11的醋酸钠溶液,由水电离出的c(H+)相等 | |
| D. | pH相同的①NaHCO3溶液②CH3COONa溶液中的c(Na+):①>② |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在常温常压下,2.8 g N2和CO的混合气体所含原子数为0.2 NA | |
| B. | 1 mol Cl2与足量Fe完全反应,转移3NA个电子 | |
| C. | 1 L 0.1 mol•L-1NaHCO3溶液中含有0.1 NA个HCO3- | |
| D. | 常温常压下,22.4L乙烯中C-H键数为4NA |
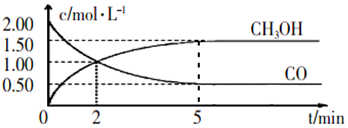
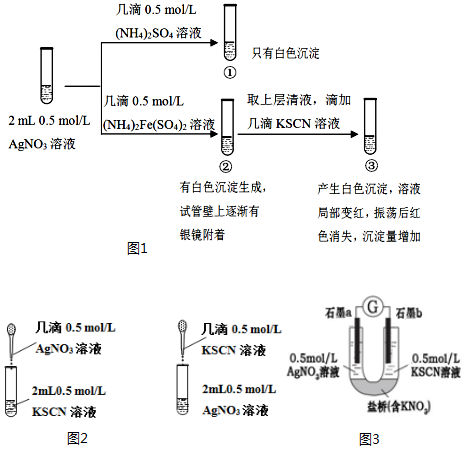
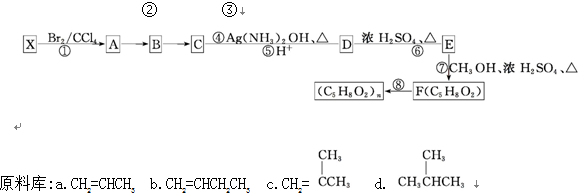
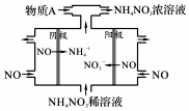 NO2是形成雾霾天气的原因之一.
NO2是形成雾霾天气的原因之一.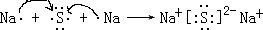 .
.
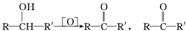 不易被氧化成羧酸
不易被氧化成羧酸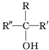 不易被氧化成醛或酮
不易被氧化成醛或酮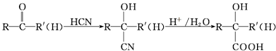
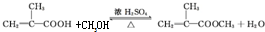 .
.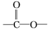 ”结构的共有6种.
”结构的共有6种.