题目内容
14.某原电池的总反应离子方程式为2Fe3++Fe═3Fe2+,不能实现该反应的原电池是( )| A. | 正极为Fe、负极为Fe,电解质溶液为FeCl3溶液 | |
| B. | 正极为Ag、负极为Fe,电解质溶液为CuSO4溶液 | |
| C. | 正极为Fe、负极为Zn,电解质溶液为Fe2(SO4)3溶液 | |
| D. | 正极为C、负极为Fe,电解质溶液为Fe(NO3)3溶液 |
分析 根据2Fe3++Fe=3Fe2+知,铁易失电子而作负极,不如铁活泼的金属或导电的非金属作正极,铁离子得电子发生还原反应,所以电解质溶液为可溶性的铁盐,以此解答该题.
解答 解:A.原电池中两个不同的电极,所以正负极不能都是Fe,故A错误.
B.铁的活泼性大于Ag,铁作负极,Ag作正极,电解质溶液为CuSO4溶液不是含Fe3+的盐溶液,故B错误.
C.铁的活泼性小于Zn,Zn作负极,Fe作正极,所以不能实现该反应的原电池,故C错误.
D.铁的活泼性强作负极,C为非金属作正极,电解质溶液为Fe(NO3)3溶液,所以是能实现该反应的原电池,故D正确.
故选D.
点评 本题考查原电池的设计及原电池的工作原理,题目难度不大,注意从氧化还原反应的角度确定原电池的电极材料及电解质溶液.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2L的戊烷所含的分子数为0.5NA | |
| B. | 28g乙烯所含共用电子对数目为5NA | |
| C. | 1 mol甲基的电子数目为7NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14g,其所含原子总数为3NA |
5.已知下列反应:①2BrO3-+Cl2=Br2+2ClO3- ②5Cl2+I2+6H2O=2HIO3+10HCl ③ClO3-+5Cl-+6H+=3Cl2+3H2O判断下列物质氧化能力强弱顺序正确的是( )
| A. | ClO3->BrO3->IO3->Cl2 | B. | ClO3->BrO3->Cl2>IO3- | ||
| C. | BrO3->ClO3->Cl2>IO3- | D. | Cl2>BrO3->ClO3->IO3- |
2.取500mL Na2CO3溶液与300mL 1mol/L盐酸反应,在不断搅拌下将碳酸钠溶液逐滴滴入盐酸中与将盐酸逐滴滴入碳酸钠溶液中,所产生气体的物质的量之比为3:2.则碳酸钠溶液的物质的量浓度( )
| A. | 0.4mol/L | B. | 0.3mol/L | C. | 0.2mol/L | D. | 0.5mol/L |
9.下列物质不能与金属钠反应的是( )
| A. | 水 | B. | 煤油 | C. | 盐酸 | D. | 乙醇 |
19.下列物质中,可作为绿色燃料的是( )
| A. | 汽油 | B. | 煤 | C. | 石油 | D. | 氢气 |
6.在下列有机物分子中,所有原子不可能处于同一平面的是( )
| A. | CH2=CH-CN | B. | CH2=CH-CH=CH2 | C. | 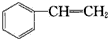 | D. | 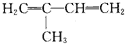 |
3.某校化学实验小组探究浓度对化学反应速率的影响,并测定(NH4)2S2O8和KI反应的化学反应速率.进行如下实验探究:
【实验原理】
(NH4)2S2O8和KI反应的离子方程式为:S2O82-+2I-=2SO42-+I2
(1)实验时,向KI、Na2S2O3和淀粉指示剂混合溶液中加入(NH4)2S2O8溶液,不断搅拌.
在反应(1)进行的同时,发生反应:2S2O32-+I2=S4O62-+2I-
(2)反应(1)生成的I2立即与S2O32-反应,生成无色的S4O62-和I-.S2O32-耗尽时,反应(1)继续生成的I2才与淀粉作用呈现蓝色.从加入(NH4)2S2O8溶液到出现蓝色的时间为△t.
【实验内容】
(1)实验小组设计的实验记录表和数据记录如下,请将表中字母表示的空格填上.
a=8.0 b=5 c=15
(2)为了使反应充分进行,减少数据误差,实验过程中应该不断进行的操作是搅拌.
(3)第①组实验的v(S2O82-)=2.5×10-5mol•(L•s)-1.
(4)根据上表数据分析,可以得到的结论有(写出一条即可)S2O82-或I-的浓度越小,反应速率越慢.
【实验原理】
(NH4)2S2O8和KI反应的离子方程式为:S2O82-+2I-=2SO42-+I2
(1)实验时,向KI、Na2S2O3和淀粉指示剂混合溶液中加入(NH4)2S2O8溶液,不断搅拌.
在反应(1)进行的同时,发生反应:2S2O32-+I2=S4O62-+2I-
(2)反应(1)生成的I2立即与S2O32-反应,生成无色的S4O62-和I-.S2O32-耗尽时,反应(1)继续生成的I2才与淀粉作用呈现蓝色.从加入(NH4)2S2O8溶液到出现蓝色的时间为△t.
【实验内容】
(1)实验小组设计的实验记录表和数据记录如下,请将表中字母表示的空格填上.
| 实 验 编 号 | ① | ② | ③ | ④ | ⑤ | |
试剂 用量 (mL) | 0.20mol•L-1(NH4)2 S2O8溶液 | 20.0 | 10.0 | b | 20.0 | 20.0 |
| 0.20mol•L-1KI溶液 | 20.0 | 20.0 | 20.0 | 10.0 | 5.0 | |
| 0.010mol•L-1 Na2S2O3溶液 | a | 8.0 | 8.0 | 8.0 | 8.0 | |
| 0.2% 淀粉溶液 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | |
| 0.20mol•L-1KNO3溶液 | 0 | 0 | 0 | 10.0 | c | |
| 0.20mol•L-1(NH4)2SO4溶液 | 0 | 10.0 | 15.0 | 0 | 0 | |
| 20℃时,反应时间△t(s) | 32 | 67 | 130 | 66 | 135 | |
| 为了使溶液的离子强度和总体积保持不变,减少的(NH4)2S2O8溶液或KI溶液的用量,分别用(NH4)2SO4溶液或KNO3溶液补足;溶液混合后体积不变 | ||||||
(2)为了使反应充分进行,减少数据误差,实验过程中应该不断进行的操作是搅拌.
(3)第①组实验的v(S2O82-)=2.5×10-5mol•(L•s)-1.
(4)根据上表数据分析,可以得到的结论有(写出一条即可)S2O82-或I-的浓度越小,反应速率越慢.
4. A到F是原子序数依次增大的前四周期元素:
A到F是原子序数依次增大的前四周期元素:
回答下列问题:
(1)写出E、F的元素符号Mg、Cr,B、C、D元素的第一电离能由大到小的顺序为N>O>C(用元素符号表示),A元素分别与B、D元素形成的两种微粒都具有与NH3相似的结构,属于等电子体,它们的化学式依次是CH3-、H3O+.
(2)在CH3Cl、C6H6、HCHO、CH3OH、CH≡CH中,碳原子采取sp2杂化的有C6H6、HCHO;应用价层电子对互斥理论,预测COCl2的空间构型为平面三角形.
(3)F元素的原子基态价层电子排布图是 .
.
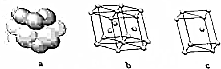
(4)E单质晶体中原子的堆积模型如图,晶胞是图中的c(填“a”、“b”或“c”);配位数是12‘若紧邻的四个E原子的中心连线构成的几何体的体积是Vcm3,E单质的密度为ρg•cm-3,则E的相对原子质量是计算式是6NA•V•ρ.
 A到F是原子序数依次增大的前四周期元素:
A到F是原子序数依次增大的前四周期元素:| A | A是原子半径最小的元素 |
| B | B基态原子的价层电子排布式为nsnnpn |
| D | D原子最外层电子数是次外层电子数的三倍 |
| E | C的三价阴离子和E的二价阳离子具有相同的电子层结构 |
| F | F元素的基态原子有六个成单电子 |
(1)写出E、F的元素符号Mg、Cr,B、C、D元素的第一电离能由大到小的顺序为N>O>C(用元素符号表示),A元素分别与B、D元素形成的两种微粒都具有与NH3相似的结构,属于等电子体,它们的化学式依次是CH3-、H3O+.
(2)在CH3Cl、C6H6、HCHO、CH3OH、CH≡CH中,碳原子采取sp2杂化的有C6H6、HCHO;应用价层电子对互斥理论,预测COCl2的空间构型为平面三角形.
(3)F元素的原子基态价层电子排布图是
 .
.(4)E单质晶体中原子的堆积模型如图,晶胞是图中的c(填“a”、“b”或“c”);配位数是12‘若紧邻的四个E原子的中心连线构成的几何体的体积是Vcm3,E单质的密度为ρg•cm-3,则E的相对原子质量是计算式是6NA•V•ρ.