题目内容
A-H分别表示中学化学中常见的一种物质,它们之间的相互转化关系如图所示(部分反应物、生成物未列出).已知:C、D、E、F、G中均含有同一种元素;A为淡黄色固体化合物;G为红褐色固体.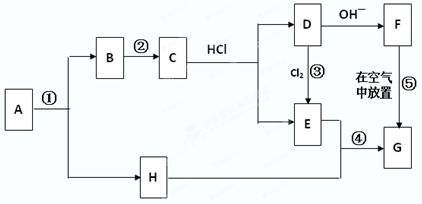
(1)写出化学式:
A: C: F:
(2)写出反应的化学方程式:
① ②
(3)写出反应的离子方程式:
③
(4)描述F→G反应的现象 .

(1)写出化学式:
A:
(2)写出反应的化学方程式:
①
(3)写出反应的离子方程式:
③
(4)描述F→G反应的现象
考点:无机物的推断
专题:
分析:C、D、E、F、G中均含有同一种元素,G为红褐色固体,且D和OH-反应生成F,F在空气中放置生成的G,可判断G为Fe(OH)3,F为Fe(OH)2,D是含有亚铁离子的可溶性盐FeCl2,D和氯气反应生成E,则E为FeCl3,C和稀盐酸反应生成亚铁盐和铁盐,则C为Fe3O4,A为淡黄色固体化合物,A为Na2O2,B为O2,H为NaOH,依此解答.
解答:
解:C、D、E、F、G中均含有同一种元素,G为红褐色固体,且D和OH-反应生成F,F在空气中放置生成的G,可判断G为Fe(OH)3,F为Fe(OH)2,D是含有亚铁离子的可溶性盐FeCl2,D和氯气反应生成E,则E为FeCl3,C为Fe3O4,A为淡黄色固体化合物,A为Na2O2,B为O2,H为NaOH,
(1)由以上分析,A为Na2O2,C为Fe3O4,F为Fe(OH)2,故答案为:Na2O2;Fe3O4;Fe(OH)2;
(2)反应①Na2O2为H2O和反应生成O2和NaOH,反应方程式为2Na2O2+2H2O=4NaOH+O2↑,反应②为Fe在氧气中燃烧生成四氧化三铁,反应方程式为3Fe+2O2
Fe3O4;故答案为:2Na2O2+2H2O=4NaOH+O2↑;3Fe+2O2
Fe3O4;
(3)反应③氯化亚铁和氯气反应,氯化亚铁不稳定易被氯气氧化生成氯化铁,反应离子方程式为2Fe2++Cl2=2Fe3++2Cl-;故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(4)F→G反应是氢氧化亚铁转化为氢氧化铁的反应,氢亚铁氧化亚铁不稳定易被氧气氧化生成氢氧化铁,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,反应现象是生成白色沉淀迅速变化为灰绿色最后变化为红褐色,故答案为:生成白色沉淀迅速变化为灰绿色最后变化为红褐色.
(1)由以上分析,A为Na2O2,C为Fe3O4,F为Fe(OH)2,故答案为:Na2O2;Fe3O4;Fe(OH)2;
(2)反应①Na2O2为H2O和反应生成O2和NaOH,反应方程式为2Na2O2+2H2O=4NaOH+O2↑,反应②为Fe在氧气中燃烧生成四氧化三铁,反应方程式为3Fe+2O2
| ||
| ||
(3)反应③氯化亚铁和氯气反应,氯化亚铁不稳定易被氯气氧化生成氯化铁,反应离子方程式为2Fe2++Cl2=2Fe3++2Cl-;故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(4)F→G反应是氢氧化亚铁转化为氢氧化铁的反应,氢亚铁氧化亚铁不稳定易被氧气氧化生成氢氧化铁,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,反应现象是生成白色沉淀迅速变化为灰绿色最后变化为红褐色,故答案为:生成白色沉淀迅速变化为灰绿色最后变化为红褐色.
点评:本题以Na、Fe、Cl元素及其化合物为载体考查了无机物推断,根据物质的颜色、物质之间的反应为突破口进行推断,熟悉常见元素化合物性质是解本题关键,铁离子的检验是考试高频点,会描述实验现象,题目难度中等.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
同温同压下,甲、乙两容器分别盛有CH4和NH3,已知它们所含氢原子个数相同,则甲、乙两容器的体积比为( )
| A、4:3 | B、5:4 |
| C、4:5 | D、3:4 |
下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A、碱性氧化物 氧化铁 Fe3O4 |
| B、酸性氧化物 碳酸气 CO |
| C、酸 硫酸 H2S |
| D、盐 纯碱 Na2CO3 |
下列实验操作中,所用仪器不合理的是( )
| A、在蒸发皿中放入NaCl溶液,加热、蒸发制取NaCl晶体 |
| B、用10ml的量筒量取5.2ml的盐酸 |
| C、用托盘天平称取25.2gNaCl |
| D、用50ml容量瓶配制100ml 0.1mol/L的盐酸 |
 硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)?2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题,
硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)?2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题,
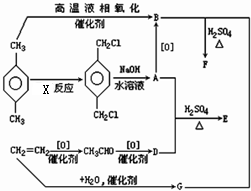 有机物E和F可用作塑料增塑剂或涂料中的溶剂,它们的分子量相等,可用以下方法合成:
有机物E和F可用作塑料增塑剂或涂料中的溶剂,它们的分子量相等,可用以下方法合成: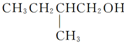 在Ag存在和加热条件下与O2反应的化学方程式:
在Ag存在和加热条件下与O2反应的化学方程式: