题目内容
16.有机物H是合成免疫抑制剂药物霉酚酸的中间体,可由如下路径合成得到.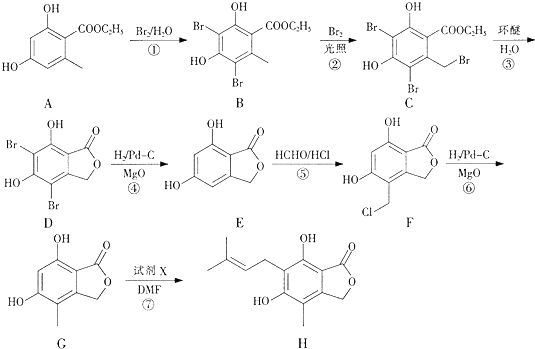
(1)有机物A中的含氧官能团的名称为酚羟基、酯基.
(2)由C转化为D的反应类型为取代反应.
(3)反应⑦除了得到有机物H外还得到HBr,试剂X的结构简式为(CH3)2C=CHCH2Br.
(4)步骤⑤可得到副产品有机物J,有机物J和有机物F互为同分异构体,写出有机物J的结构简式:
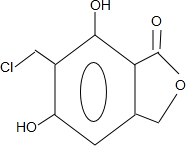 (任写一种).
(任写一种).(5)E的一种同分异构体满足下列条件:
Ⅰ.可以发生银镜反应,且能够与NaHCO3反应产生CO2;
Ⅱ.是芳香族化合物,且核磁共振氢谱图显示分子中有4种不同化学环境的氢.
写出该同分异构体的结构简式:
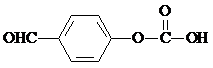 或
或 .
.(6)已知:直接与苯环相连的卤素原子难以与NaOH水溶液发生取代反应.根据已有知识并结合相关信息,写出以$\stackrel{HBr}{→}$HCHO为原料制备$→_{△}^{NaOH_{2}}$合成路线流程图(无机试剂任用).合成路线流程图示例如下:
CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=C2H$\stackrel{Br_{2}}{→}$
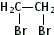
分析 由合成H的路线图可知,反应①是酚羟基临位上的溴代反应,反应②是甲基上的卤代反应,反应③是取代反应,生成酯基,反应④是去掉苯环上的溴原子,反应⑤是在苯环上引入-CH2Cl,因为苯环上有两个空位,所以F可能存在同分异构体,反应⑥是使-CH2Cl生成-CH3的反应,反应⑦是在苯环的另一个空位上引入(CH3)2C=CHCH2-;以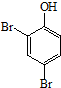 、HCHO为原料制备
、HCHO为原料制备 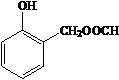 ,需先在酚羟基的临位引入-CH2Cl,在水解生成-OH,去掉Br,醛基与甲酸酯化生成
,需先在酚羟基的临位引入-CH2Cl,在水解生成-OH,去掉Br,醛基与甲酸酯化生成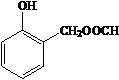 ,据此分析.
,据此分析.
解答 解:(1)由A的结构简式可知,其含有的官能团有酚羟基、酯基,故答案为:酚羟基、酯基;
(2)反应③是取代反应,生成酯基和CH2CH2Br,故答案为:取代反应;
(3)反应⑦是在苯环的另一个空位上引入(CH3)2C=CHCH2CH2-,还得到HBr,说明是G与(CH3)2C=CHCH2Br发生取代反应,
故答案为:(CH3)2C=CHCH2Br;
(4)反应⑤是在苯环上引入-CH2Cl,因为苯环上有两个空位,所以F可能存在同分异构体 ,
,
故答案为: ;
;
(5)E除苯环外还有4个氧原子2个碳原子,E的同分异构体可以发生银镜反应,说明含有醛基,能够与NaHCO3反应产生CO2,说明含有羧基,是芳香族化合物,且核磁共振氢谱图显示分子中有4种不同化学环境的氢,说明羧基和醛基在对位,E的同分异构体为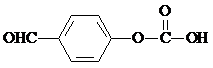

故答案为: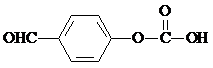

(6)以 、HCHO为原料制备
、HCHO为原料制备 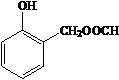 ,需先在酚羟基的临位引入-CH2Cl,在水解生成-OH,去掉Br,醛基与甲酸酯化生成
,需先在酚羟基的临位引入-CH2Cl,在水解生成-OH,去掉Br,醛基与甲酸酯化生成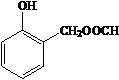 ,合成路线流程图为:
,合成路线流程图为:
故答案为: .
.
点评 本题考查了有机物的推断,根据各物质的结构采用正逆结合的方法进行推断,推断时要根据反应条件结合解答,为高考热点题型,要注意以教材为原型采用知识迁移的方法进行分析解答问题,题目难度不大.

| A. | 2 4 3 2 2 6 | B. | 0 2 1 0 1 2 | ||
| C. | 2 0 1 2 0 2 | D. | 2 2 2 2 1 4 |
| A. | 碳酸氢钠溶液中滴入足量氢氧化钙溶液:HCO3-+OH-=CO32-+H2O | |
| B. | 硅酸钠溶液与足量CO2反应:SiO32-+CO2+H2O=H2SiO3↓+CO32- | |
| C. | FeBr2溶液中通入足量的Cl2:2Fe2++Cl2=2Fe3++2Cl- | |
| D. | 新制的氧化铝可溶于氢氧化钠溶液:Al2O3+2OH-=2AlO2-+H2O |
| A. | 32g O2中含有32NA个电子 | |
| B. | 22.4L N2含有阿伏加德罗常数个氮分子 | |
| C. | 在标准状况下,22.4L水的质量约为18g | |
| D. | 常温常压下22g的CO2与标准状况下11.2L HCl含有相同的分子数 |
| A. | 铜 | B. | 二氧化碳 | C. | 金刚石 | D. | 氯化钠 |

| A. | ①中阳极处能产生使湿润淀粉KI试纸变蓝的气体 | |
| B. | ②中待镀铁制品应与电源正极相连 | |
| C. | ③中钢闸门应与外接电源的正极相连,称为牺牲阳极的阴极保护法 | |
| D. | ④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
| A. | MgF2的电子式: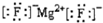 | B. | 二甲醚的结构式:CH3-O-CH3 | ||
| C. | NH3的球棍模型: | D. | 氧原子的结构示意图: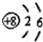 |
 蛇纹石可用于生产氢氧化镁,简要工艺流程如下:
蛇纹石可用于生产氢氧化镁,简要工艺流程如下:Ⅰ.制取粗硫酸镁:用酸液浸泡蛇纹石矿粉,过滤;并在常温常压下结晶,制得粗硫酸镁(其中常含有少量
Fe3+、Al3+、Fe2+等杂质离子).
Ⅱ.提纯粗硫酸镁:将粗硫酸镁在酸性条件下溶解,加入适量的0.1 mol/L H2O2溶液,再调节溶液pH至7~8,并分离提纯.
Ⅲ.制取氢氧化镁:向步骤Ⅱ所得溶液中加入过量氨水.
已知:金属离子氢氧化物沉淀所需pH如下表所示:
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
A.MgO B.Na2CO3 C.蒸馏水
(2)工业上,常通过测定使铁氰化钾(K3[Fe(CN)6])溶液不变色所需H2O2溶液的量来确定
粗硫酸镁中Fe2+的含量.已知,测定123 g粗硫酸镁样品所消耗的0.1 mol/L H2O2溶液的体积如下表所示:
| 平行测定数据 | 平均值 | ||||
| 实验编号 | 1 | 2 | 3 | 4 | |
| 消耗H2O2溶液的体积/mL | 0.32 | 0.30 | 0.30 | 0.32 | 0.31 |
①步骤Ⅲ中制备氢氧化镁反应的离子方程式为Mg2++2NH3•H2O═Mg(OH)2↓+2NH4+.
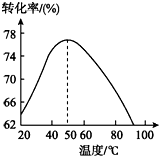
②根据图中所示50℃前温度与Mg2+转化率之间的关系,可判断此反应是吸热(填“吸热”或“放热”)反应.
③图中,温度升高至50℃以上Mg2+转化率下降的可能原因是温度过高时,氨水受热分解,浓度降低,Mg2+转化率下降.
④Ksp表示沉淀溶解平衡的平衡常数.已知:
Mg(OH)2(s)?Mg2+(aq)+2OH-(aq) Ksp=c(Mg2+)•c2(OH-)=5.6×10-12
Ca(OH)2(s)?Ca2+(aq)+2OH-(aq) Ksp=c(Ca2+)•c2(OH-)=4.7×10-6
若用石灰乳替代氨水,能(填“能”或“不能”)制得氢氧化镁,理由是Mg(OH)2的溶解度小于Ca(OH)2,可发生沉淀的转化.