题目内容
6.除去下列括号内杂质的试剂或方法错误的是( )| A. | HNO3溶液(H2SO4),适量BaCl2溶液,过滤 | |
| B. | CO2(SO2),酸性KMnO4溶液、浓硫酸,洗气 | |
| C. | FeCl2溶液(FeCl3),铁粉,过滤 | |
| D. | CO(CO2),氢氧化钠溶液,洗气 |
分析 A.加入氯化钡生成HCl,引入新杂质;
B.SO2有还原性,可被高锰酸钾氧化为硫酸除去;
C.氯化铁与铁反应生成氯化亚铁;
D.二氧化碳可与氢氧化钠溶液反应.
解答 解:A.HNO3溶液中混有H2SO4时,加入适量BaCl2溶液,与H2SO4反应生成BaSO4沉淀和HCl,除去了H2SO4,使得硝酸中又混入了HCl杂质,应加入硝酸钡溶液,过滤,故A错误;
B.SO2有还原性,可被高锰酸钾氧化为硫酸除去,再通过浓硫酸洗气,故B正确;
C.氯化铁与铁反应生成氯化亚铁,可除去杂质,故C正确;
D.二氧化碳可与氢氧化钠溶液反应,可用于除杂,故D正确.
故选A.
点评 本题考查物质的分离、提纯,侧重于学生的分析能力、实验能力和评价能力的考查,难度不大,注意把握物质的性质的异同,注意除杂时不能引入新的杂质.

练习册系列答案
相关题目
16.既能发生银镜反应、又能发生水解反应的是( )
| A. | 葡萄糖 | B. | 麦牙糖 | C. | 淀粉 | D. | 蔗塘 |
17.下列离子方程式书写正确的是( )
| A. | 在100 mL浓度为1 mol•L-1的 Fe(NO3)3的溶液中通入足量SO2:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| B. | 在100 mL浓度为2 mol•L-1的FeI2的溶液中通入标准状况下5.6 L的Cl2:4Fe2++6I-+5Cl2═4Fe3++3I2+10Cl- | |
| C. | 向NaHCO3溶液中加入过量的澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
14.用高氯酸、硫酸、氢碘酸、醋酸、钠盐、钾盐、铵盐、钡盐相互反应,符合离子方程式2H++CO32-═CO2↑+H2O的反应有( )
| A. | 6个 | B. | 8个 | C. | 9个 | D. | 12个 |
1.下列说法中正确的是( )
| A. | 有单质参加的反应一定是氧化还原反应 | |
| B. | 化学反应速率变化时,化学平衡一定发生转移 | |
| C. | 化学反应速率和限度均可通过改变相应的化学反应条件而改变 | |
| D. | 自发进行的氧化还原反应理论上可以设计成原电池,而电解池反应一定是非自发进行的氧化还原反应 |
15.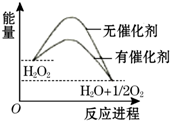 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )| A. | 加入催化剂,减小了反应的热效应 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | H2O2分解的热效应△H<0 | |
| D. | 反应物的总能量高于生成物的总能量 |