题目内容
常见的纽扣式电池为银锌电池.它用不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒内靠正极壳一端填充由Ag2O和少量石墨组成的正极活性材料,负极盖一端填充锌汞合金作负极活性材料,电解质溶液为浓KOH,溶液两边用羧甲基纤维素作隔膜.锌银电池的负极是Zn,正极是Ag2O,电解质是KOH,其总的反应式为:
Zn+Ag2O=2Ag+ZnO.
(1)写出正、负极的电极反应式:负极: .正极: .
(2)电池工作过程中,电池负极溶液的pH (填“增大”、“减小”或“不变”)
Zn+Ag2O=2Ag+ZnO.
(1)写出正、负极的电极反应式:负极:
(2)电池工作过程中,电池负极溶液的pH
考点:化学电源新型电池
专题:
分析:(1)该原电池反应式中,Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,所以Zn作负极、Ag2O作正极,负极上锌失电子发生氧化反应、正极上氧化银得电子发生还原反应;
(2)放电过程中,负极上氢氧根离子参加反应,导致溶液中氢氧根离子浓度减小,据此分析解答.
(2)放电过程中,负极上氢氧根离子参加反应,导致溶液中氢氧根离子浓度减小,据此分析解答.
解答:
解:(1)该原电池反应式中,Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,所以Zn作负极、Ag2O作正极,负极上锌失电子发生氧化反应、正极上氧化银得电子发生还原反应,负极反应式为Zn-2e-+2OH-=ZnO+H2O、正极反应式为Ag2O+2e-+H2O=2Ag+2OH-,
故答案为:Zn-2e-+2OH-=ZnO+H2O;Ag2O+2e-+H2O=2Ag+2OH-;
(2)放电过程中,负极反应式为Zn-2e-+2OH-=ZnO+H2O,负极上氢氧根离子参加反应,导致溶液中氢氧根离子浓度减小,所以溶液的pH减小,故答案为:减小.
故答案为:Zn-2e-+2OH-=ZnO+H2O;Ag2O+2e-+H2O=2Ag+2OH-;
(2)放电过程中,负极反应式为Zn-2e-+2OH-=ZnO+H2O,负极上氢氧根离子参加反应,导致溶液中氢氧根离子浓度减小,所以溶液的pH减小,故答案为:减小.
点评:本题考查化学电源新型电池,明确原电池中元素化合价升降与正负极的关系是解本题关键,难点是电极反应式的书写,要结合电解质溶液酸碱性书写,题目难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
某溶液中只含有Na+、CO32-、Cl-,检验该溶液中Cl-的方法正确的是( )
| A、加入足量稀HNO3酸化的AgNO3溶液 |
| B、先加入足量BaCl2溶液,过滤,再加入AgNO3溶液 |
| C、先加入足量稀H2SO4,再加入AgNO3溶液 |
| D、先加入稀盐酸,再加入AgNO3溶液 |
为除去FeSO4溶液中的Fe2(SO4)3和CuSO4,最好选用( )
| A、铁粉 | B、浓氨水 |
| C、镁粉 | D、烧碱溶液 |
下列说法中正确的是( )
| A、常温下,淀粉遇I- 变蓝色 |
| B、油脂水解可得到氨基酸和甘油 |
| C、所有烷烃和蛋白质中都只存在碳碳单键 |
| D、淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖 |
在含有1mol KAl(SO4)2的明矾溶液中滴入含有2mol溶质的Ba(OH)2溶液,充分反应后,当SO42-全部转化为BaSO4沉淀时,铝元素的存在形式是( )
| A、Al(OH)3和Al3+ |
| B、Al(OH)3和AlO2- |
| C、Al3+、Al(OH)3 和AlO2- |
| D、全部为AlO2- |
在密闭容器中,一定条件下进行如下反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.4kJ?mol-1
达到平衡后,为提高反应的速率和NO的转化率,采取的正确措施是( )
达到平衡后,为提高反应的速率和NO的转化率,采取的正确措施是( )
| A、加催化剂同时升高温度 |
| B、加催化剂同时增大压强 |
| C、升高温度同时充入氮气 |
| D、降低温度同时增大压强 |

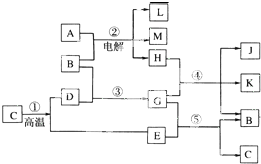 如图所示,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应.
如图所示,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应.