��Ŀ����
2����ҵ�����÷���м�����������������������ȣ�������ʽ������[Fe��OH��SO4]�Ĺ����������£�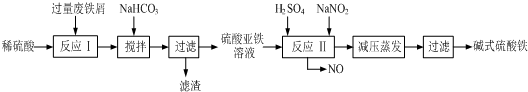
��֪������������������������ʽ����ʱ��Һ��pH���±���
| ������ | Fe��OH��3 | Fe��OH��2 | Al��OH��3 |
| ��ʼ���� | 2.3 | 7.5 | 3.4 |
| ��ȫ���� | 3.2 | 9.7 | 4.4 |
��1����������NaHCO3��Ŀ���ǵ���pH����ȥ��Һ��Al3+��ʹ��Һ��Al3+��������������������ù����С����衱��������ʹ��Ӧ���ֽӴ����ӿ췴Ӧ���ʣ�ʹ��Ӧ��ֽ��У�
��2����Ӧ���е����ӷ���ʽΪFe2++2H++NO2-=Fe3++NO��+H2O��Fe2++H2O+NO2-=Fe��OH��2++NO��+H+����ʵ�������У���Ӧ��ͬʱͨ��O2�Լ���NaNO2��������O2��������2H2O+4NO+O2=4HNO3����2NO+O2=2NO23NO2+H2O=2HNO3+NO�������û�ѧ����ʽ��ʾ��
��3�������м�ʽ��������Һ����ʱ��Ҫ�ڳ��¼�ѹ�����µ�ԭ���Ƿ�ֹ����ʱ�¶ȹ��ߣ���ʽ��������һ��ˮ������Fe��OH��3��
��4����ҽҩ�ϳ����������������ᡢ����Ļ��Һ��Ӧ�Ʊ���ʽ�������������ҹ�����������Ʒ�в��ú���Fe2+��NO3-��Ϊ�������ò�Ʒ���Ƿ���Fe2+��Ӧʹ�õ��Լ�ΪD������д��ĸ��
A����ˮ B��KSCN��Һ C��NaOH��Һ D������KMnO4��Һ��
���� ����м�к��������������������ȣ�����������м����ϡ�����У�������Ӧ Fe+H2SO4=FeSO4+H2����Al2O3+3H2SO4=Al2��SO4��3+3H2O��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��Fe2��SO4��3+Fe=3FeSO4��Ȼ��ӦI�м���NaHCO3�����裬������Һ��pH��������ӦAl3++3HCO3-=Al��OH��3��+3CO2�������������гɷ���Al��OH��3�����˵õ�����������������������Һ�м���ϡ�����NaNO2�����������£�NaNO2��FeSO4����������ԭ��Ӧ���������ӡ�NO������Һ����Ũ�������˵õ���ʽ��������
��1��NaHCO3�ܺ������ӷ�Ӧ��������Һ��pH���ù����С����衱�ܼӿ췴Ӧ���ʣ�
��2�����������£��������Ӻ�����������ӷ���������ԭ��Ӧ���������ӡ�NO��ˮ������������NO���ɶ�������������������ˮ��Ӧ�������
��3���¶ȸ�ʱ����ʽ��������ˮ����������������
��4���������Ը��������Һ�����軯����Һ�����������ӣ�
��� �⣺����м�к��������������������ȣ�����������м����ϡ�����У�������Ӧ Fe+H2SO4=FeSO4+H2����Al2O3+3H2SO4=Al2��SO4��3+3H2O��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��Fe2��SO4��3+Fe=3FeSO4��Ȼ��ӦI�м���NaHCO3�����裬������Һ��pH��������ӦAl3++3HCO3-=Al��OH��3��+3CO2�������������гɷ���Al��OH��3�����˵õ�����������������������Һ�м���ϡ�����NaNO2�����������£�NaNO2��FeSO4����������ԭ��Ӧ���������ӡ�NO������Һ����Ũ�������˵õ���ʽ��������
��1��NaHCO3�ܺ������ӷ�Ӧ��������Һ��pH���Ӷ�ʹ������ת��Ϊ���������������ù����С����衱��ʹ��Ӧ���ֽӴ������Լӿ췴Ӧ���ʣ�ʹ��Ӧ��ֽ��У�
�ʴ�Ϊ������pH����ȥ��Һ��Al3+��ʹ��Һ��Al3+�������������������ʹ��Ӧ���ֽӴ����ӿ췴Ӧ���ʣ�ʹ��Ӧ��ֽ��У�
��2�����������£��������Ӻ�����������ӷ���������ԭ��Ӧ���������ӡ�NO��ˮ�����ӷ���ʽΪFe2++2H++NO2-=Fe3++NO��+H2O ��Fe2++H2O+NO2-=Fe��OH��2++NO��+H+������������NO���ɶ�������������������ˮ��Ӧ�������ᣬ��Ӧ����ʽΪ2H2O+4NO+O2=4HNO3����2NO+O2=2NO2 3NO2+H2O=2HNO3+NO����
�ʴ�Ϊ��Fe2++2H++NO2-=Fe3++NO��+H2O ��Fe2++H2O+NO2-=Fe��OH��2++NO��+H+��
2H2O+4NO+O2=4HNO3����2NO+O2=2NO2 3NO2+H2O=2HNO3+NO����
��3���¶ȸ�ʱ����ʽ��������ˮ��������������������Ϊ��ֹ����ʱ�¶ȹ��߶����¼�ʽ��������һ�����������������������ü�ѹ������
�ʴ�Ϊ����ֹ����ʱ�¶ȹ��ߣ���ʽ��������һ��ˮ������Fe��OH��3��
��4���������Ը��������Һ�����軯����Һ�����������ӣ����������ܽ����Ը��������Һ��ԭ��ʹ���Ը��������Һ��ɫ����������NaOH��Һ��Ӧ���������ԣ���KSCN��Һ����Ӧ���ʴ�Ϊ��D��
���� ���⿼�������Ʊ���Ϊ��Ƶ���㣬���ؿ���ѧ����ɻ�ȡ��Ϣ��������Ϣ��֪ʶ�ۺ�������������ȷԪ�ػ��������ʡ����ʷ����ᴿ�����ǽⱾ��ؼ����漰������ԭ��Ӧ�����Ӽ����֪ʶ�㣬֪�������ӡ��������ӵļ��鷽����������Ŀ�ѶȲ���

 ����ʦ��Сһ����ʦ������ҵϵ�д�
����ʦ��Сһ����ʦ������ҵϵ�д� ���100�ֵ�Ԫ�Ż�������ϵ�д�
���100�ֵ�Ԫ�Ż�������ϵ�д�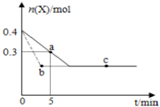 �ں���2L�ܱ�������ͨ������X��������Ӧ��2X��g���TY��g����H��0��X�����ʵ���n��x����ʱ��t�仯��������ͼ��ʾ��ͼ�е������߷ֱ���������������Σ�������������ȷ���ǣ�������
�ں���2L�ܱ�������ͨ������X��������Ӧ��2X��g���TY��g����H��0��X�����ʵ���n��x����ʱ��t�仯��������ͼ��ʾ��ͼ�е������߷ֱ���������������Σ�������������ȷ���ǣ�������| A�� | ʵ�߱�ʾʹ�ô��������� | |
| B�� | b��c���������Ӧ����Ӧ�����´ﵽ������� | |
| C�� | ��Ӧ�ӿ�ʼ��a���ƽ����Ӧ���ʿɱ�ʾΪv��Y��=0.01mol/��L•min�� | |
| D�� | ��Ӧ���е�a��ʱ�ų����������ڷ�Ӧ���е�b��ʱ�ų������� |
| A�� | NH4Cl��s���TNH3��g��+HCl��g�������²����Է����У�˵���÷�Ӧ�ġ�H��0 | |
| B�� | ��п����Ʒ�Ʋ����������Ʒ������ǰ���������⣬�����������෴ | |
| C�� | ����N2��g��+3H2��g��?2NH3��g������������������ʱ��ѹ���������ʹѹǿ��������Ӧ���淴Ӧ�����Լ�H2��ƽ��ת���ʾ����� | |
| D�� | 25��ʱNH3•H2Oϡ��Һ�У���ˮϡ��$\frac{c��{H}^{+}��•c��N{H}_{3}•{H}_{2}O��}{c��N{H}_{4}^{+}��}$��ֵ���� |
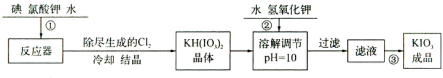
��1����֪����ٷ�Ӧ�������ķ�ӦΪ��6I2+11KClO3+3H2O=6KH��IO3��2+5KCl+3Cl2����
�÷�Ӧ�Ļ�ԭ����ΪKCl��Cl2��
��2�������±�����ص��ܽ�ȣ������۵õ�����ؾ��壬�㽨��ķ����ǽ��½ᾧ��
| �¶�/�� | 20 | 40 | 60 | 80 |
| KIO3g/100gˮ | 8.08 | 12.6 | 18.3 | 24.8 |
��3������֪��
�ⶨ�ӵ�ʳ���е�ĺ�����ѧ������Ƶ�ʵ�鲽�����£�
a��ȷ��ȡwgʳ�Σ�����������ˮʹ����ȫ�ܽ⣻
b����ϡ�����ữ������Һ���������KI��Һ��ʹKIO3��KI��Ӧ��ȫ��
c���Ե���Ϊָʾ������μ������ʵ���Ũ��Ϊ2.00��10-3mol•L-1��Na2S2O3��Һ10.0mL��ǡ�÷�Ӧ��ȫ����ӵ�ʳ����Ʒ�еĵ�Ԫ�غ�����$\frac{1270}{3w}$mg•kg-1���Ժ�w�Ĵ���ʽ��ʾ����
��ѧ�����ֽ���������ʵ�飺
| �������� | ʵ������ |
| ȡ1g������NaCl����3mLˮ�����Һ | ��Һ�ޱ仯 |
| ����5�ε�����Һ��1mL0.1mol•L-1KI��Һ���� | ��Һ�ޱ仯 |
| Ȼ���ٵ���1mol•L-1��H2SO4������� | ��Һ����ɫ |
����ѧ���ҵ�ʵ���������ѧ����ʵ����������Ҫ���ۣ�ƫ������I-�ᱻ�����е�O2����ΪI2 ��
��4��ijѧϰС��Լӵ��ν�������ʵ�飺ȡһ����ij�ӵ��Σ����ܺ���KIO3��KI��Mg2+��Fe3+��������������ˮ�ܽ⣬����ϡ�����ữ����������Һ��Ϊ3�ݣ���һ����Һ�еμ�KSCN��Һ���Ժ�ɫ���ڶ�����Һ�м�����KI���壬��Һ�Ե���ɫ����CCl4��ȡ���²���Һ���Ϻ�ɫ����������Һ�м�������KIO3����μӵ����Լ�����Һ����ɫ��
�ٸ�������ʵ�����ӵ����п��ܺ��е������в���ȷ������Mg2+��
�ڵڶ�����Һ�м�������KI�����Ӧ�����ӷ���ʽΪ2Fe3++2I-=2Fe2++I2��IO3-+5I-+6H+�T3I2+3H2O��
 �ں�����������ʼʱ�ݻ���Ϊ5L�ļס������ܱ������У���Ϊ������������Ϊ��ѹ�������������з�Ӧ��N2��g��+3H2��g��?2NH3��g����H2=-92.4kJ/mol���й����ݼ��ض�ƽ��״̬������
�ں�����������ʼʱ�ݻ���Ϊ5L�ļס������ܱ������У���Ϊ������������Ϊ��ѹ�������������з�Ӧ��N2��g��+3H2��g��?2NH3��g����H2=-92.4kJ/mol���й����ݼ��ض�ƽ��״̬������| ���� | ��ʼͶ�� | ��ƽ��ʱ | |||
| �� | 2molN2 | 3molH2 | 0molNH3 | 1.5molNH3 | |
| �� | amolN2 | bmolH2 | 0molNH3] | 1.2molNH3 | |
��ʼʱ���е�ѹǿ�Ǽ�������0.8�����ҵ�ƽ�ⳣ��Ϊ107��mol/L��-2
��2�������ܱ������п��Է��������ķֽⷴӦ����ƽ����ı��±��з�Ӧ����x�����и�����y��x��������������bc��ѡ����ţ���
| ѡ�� | a | b | c | d |
| x | �¶� | �¶� | ����H2�����ʵ��� | ���백�������ʵ��� |
| y | ��������ƽ����Է������� | ƽ�ⳣ��K | ���������ܶ� | ��ƽ��ʱ������ת���� |
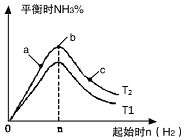
������T2��T1�Ĺ�ϵ�ǣ�T2����T1������ڡ������ڡ������ڡ�����ȷ��������
��a��b��c�����У�N2ת������ߵ���c������ĸ����
���������ݻ�Ϊ1L��T2������ʼ��ϵ�м���1mol N2��3molH2������5min��Ӧ�ﵽƽ��ʱH2��ת����Ϊ60%����NH3�ķ�Ӧ����Ϊ0.24mol��L-1��min-1����������������䣬����ʼʱ�������ڷ���2mol N2��6mol H2����ƽ���ų�������ΪQ����Q��110.88kJ�����������������=������
| A�� | 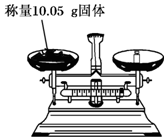 | B�� | 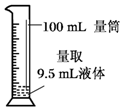 | ||
| C�� | 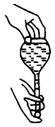 �������ƿ�Ƿ�©ˮ | D�� | 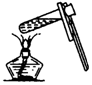 ��Һ����� |