题目内容
在反应3NO2+H2O═2HNO3+NO中,发生还原反应和发生氧化反应的物质质量之比为( )
| A、3:1 | B、1:3 |
| C、1:2 | D、2:1 |
考点:氧化还原反应
专题:
分析:由3NO2+H2O═2HNO3+NO可知,反应中只有氮元素的化合价发生变化,由+4价升高为+5价,由+4价降低为+2价,所以NO2既是氧化剂也是还原剂,氧化剂对应还原产物,还原剂对应氧化产物,依据氧化产物与还原产物的物质的物质的量解答.
解答:
解:由3NO2+H2O═2HNO3+NO可知,反应中只有氮元素的化合价发生变化,由+4价升高为+5价,由+4价降低为+2价,所以NO2既是氧化剂也是还原剂,氧化剂对应还原产物,NO为还原产物,物质的量为1mol;还原剂对应氧化产物,硝酸为氧化产物,物质的量为2mol,所以氧化剂与还原剂物质的量之比为:1:2,即发生还原反应和发生氧化反应的物质质量之比为1:2;
故选:C.
故选:C.
点评:本题考查氧化还原反应计算、氧化还原反应概念,理解基本概念,关键根据产物中化合价判断起氧化剂与还原剂的NO2物质的量之比,题目难度不大.

练习册系列答案
相关题目
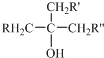 中的-OH不能被氧化.
中的-OH不能被氧化.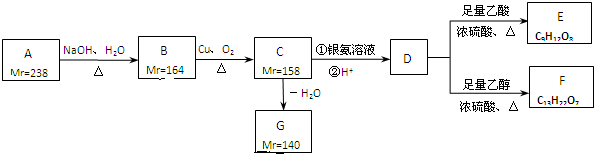
 结构的有机物可被酸性高锰酸钾溶液氧化成二元醇,如:CH2=CH2
结构的有机物可被酸性高锰酸钾溶液氧化成二元醇,如:CH2=CH2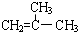 )为原料合成环状化合物F和高分子化合物E和G.
)为原料合成环状化合物F和高分子化合物E和G.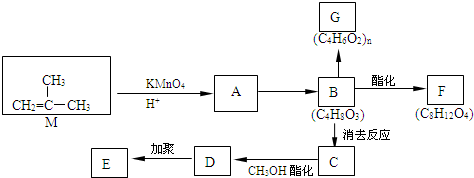
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此回答下列问题:
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此回答下列问题: