题目内容
5. 硼元素在化学中有很重要的地位,硼及其化合物广泛应用于永磁材料、超导材料、复合材料等高新材料领域.
硼元素在化学中有很重要的地位,硼及其化合物广泛应用于永磁材料、超导材料、复合材料等高新材料领域.(1)写出硼元素基态原子的电子排列图1s22s22p1.
(2)B、N、O 元素的第一电离能由大到小的顺序为N>O>B(用元素符号表示).
(3)与三氯化硼互为等电子体的一种分子的化学式为SO3.
(4)磷化硼(BP)是一种磨材料.它是由三溴化硼和三溴化磷在氢气气氛中,高温(>75℃)下制得的.它的晶体结构单元与金刚石类似.写出生成BP的反应方程式BBr3+PBr3+3H2$\frac{\underline{\;高温\;}}{\;}$BP+6HBr;已知BP晶胞参数为a pm,则BP密度的表达式为$\frac{4×\frac{M}{{N}_{a}}}{(\sqrt{2}a×1{0}^{-10})^{3}}$g/cm3(用含a、Na的式子表示).
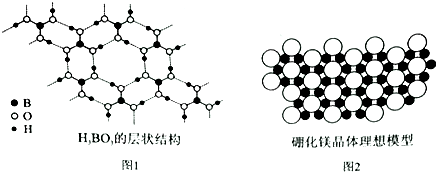
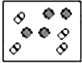
(5)正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子间通过氢键相连(如图l)
①1mol H3BO3的晶体中有3mol氢键.
②硼酸溶于水后,电离生成少量[B(OH)4]-和H+离子.[B(OH)4]-中B原子杂化类型为正四面体型.
(6)科学家发现硼化镁在39K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列-.如图2是该晶体微观空间取出的部分原子在同一平面上的投影,硼化镁的化学式为MgB2.
分析 (1)B原子核外有5个电子,根据构造原理书写其基态原子核外电子排布式;
(2)同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素的第一电离能大于相邻元素;
(3)原子个数相等、价电子数相等的微粒互为等电子体,等电子体的结构相似;
(4)根据元素守恒可写出合成磷化硼的化学反应方程式;根据图知,该晶胞是面心立方最密堆积,若该晶体中最邻近的两个P原子之间的距离为a pm,晶胞的棱长=$\sqrt{2}$apm,该晶胞中P原子个数=$8×\frac{1}{8}$+6×$\frac{1}{2}$=4,B原子个数为4,晶胞密度=$\frac{4×\frac{M}{Na}}{(\sqrt{2}a×1{0}^{-10})^{3}}$;
(5)利用均摊法计算含1molH3BO3的晶体中的氢键;[B(OH)4]-中B原子的价层电子对数分析;
(6)1个B原子为3个Mg原子共用,1个Mg原子为6个B原子共用,利用均摊法计算硼原子和镁原子的个数比.
解答 解:(1)B原子核外有5个电子,根据构造原理书写其基态原子核外电子排布式为1s22s22p1,故答案为:1s22s22p1;
(2)同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素的第一电离能大于相邻元素,所以三种元素的第一电离能由大到小的顺序为N>O>B,故答案为:N>O>B;
(3)原子个数相等、价电子数相等的微粒互为等电子体,可知SO3等符合,故答案为:SO3(其他合理答案也对);
(4)根据元素守恒可知由三溴化硼和三溴化磷在氢气中高温反应合成磷化硼的化学反应方程式为BBr3+PBr3+3H2$\frac{\underline{\;高温\;}}{\;}$BP+6HBr,
根据图知,该晶胞是面心立方最密堆积,若该晶体中最邻近的两个P原子之间的距离为a pm,晶胞的棱长=$\sqrt{2}$apm,该晶胞中P原子个数=$8×\frac{1}{8}$+6×$\frac{1}{2}$=4,B原子个数为4,晶胞密度=$\frac{4×\frac{M}{{N}_{a}}}{(\sqrt{2}a×1{0}^{-10})^{3}}$,故答案为:BBr3+PBr3+3H2$\frac{\underline{\;高温\;}}{\;}$BP+6HBr;$\frac{4×\frac{M}{{N}_{a}}}{(\sqrt{2}a×1{0}^{-10})^{3}}$;
(5)一个H3BO3分子对应着6个氢键,一个氢键对应着2个H3BO3分子,因此含有1 molH3BO3分子的晶体中有3mol氢键,[B(OH)4]-中B原子形成4个共价键,则B原子的价层电子对数为4,为sp3杂化,没有孤电子对,空间结构为正四面体型;
故答案为:3;正四面体型;
(6)根据投影可知,1个B原子为3个Mg原子共用,故属于一个Mg原子的B原子为$\frac{1}{3}$;1个Mg原子为6个B原子共用,故用于一个B原子的Mg原子为$\frac{1}{6}$.由此可知Mg镁硼原子个数比=1:2,故硼化镁的化学式为MgB2,故答案为:MgB2.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、等电子体、晶体类型判断等知识点,明确基本原理、基本计算机物质空间结构是解本题关键,侧重考查学生分析判断及计算能力,题目难度中等.

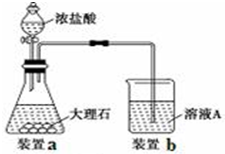
(1)试剂:a.浓硫酸 b.氢氧化钠 c.生石灰 d.碳酸钠 e.水 f.浓溴水
方法:A.过滤 B.分液 C.蒸馏
| 要提纯的物质(杂质) | C2H5OH (H2O) | CH3CH2OH (CH3COOH) | C6H5Br (Br2) | C6H6 (C6H5OH) |
| 选用试剂(1) | c | b或d | b | b |
| 分离方法(2) | C | C | B | B |
| A. | 1mol Fe与1mol Cl2反应时转移的电子数目为3NA | |
| B. | 3g C18O和14CO的混合物中所含电子、中子数目为1.4NA | |
| C. | 0℃、101kPa下,0.1mol 乙炔和甲醛(HCHO)的混合物中含有C-H数目为0.2NA | |
| D. | 50ml 18mo•L-1浓H2SO4与足量的Cu充分反应,能收集到SO2的分子数目为0.45NA |
| A. | 以煤、石油和天然气为主要原料生产的合成材料是塑料、合成橡胶、合成纤维 | |
| B. | 煤是工业上获得芳香烃的一种重要来源 | |
| C. | 石油的裂解是为了提高轻质油(例如汽油)的产量 | |
| D. | 天然气的主要成分是甲烷,属于不可再生资源 |
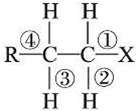
| A. | 发生水解反应时,被破坏的键是①和③ | |
| B. | 发生消去反应时,被破坏的键是①和③ | |
| C. | 发生水解反应时,被破坏的键是①和④ | |
| D. | 发生消去反应时,被破坏的键是①和② |



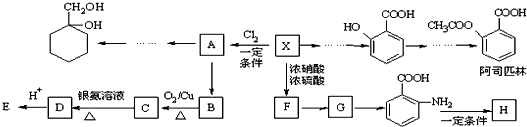
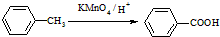
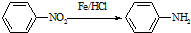 (苯胺,易被氧化)
(苯胺,易被氧化) ,F→G的反应类型是氧化反应.
,F→G的反应类型是氧化反应. .
.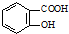 的同分异构体的结构简式
的同分异构体的结构简式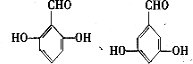 .(写出2种)
.(写出2种)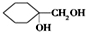 ,请设计合成路线,要求不超过4步(无机试剂任选).注:合成路线的书写格式参照如下示例流程图:
,请设计合成路线,要求不超过4步(无机试剂任选).注:合成路线的书写格式参照如下示例流程图: