题目内容
7.一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)?N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
(1)在该温度下,反应的化学平衡常数表达式为:$K=\frac{{c({N_2}{O_4})}}{{{c^2}{{(N{O_2})}^{\;}}}}$
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率:0.1mol•L-1•s-1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:t3
(4)t1时,正反应速率>(填“>”、“<”或“=”)逆反应速率.
分析 (1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;
(2)由图可知,从t1至t2时N2O4的物质的量变化量为4mol-3mol=1mol,根据v=$\frac{\frac{△n}{V}}{△t}$计算v(N2O4);
(3)到达平衡时,反应混合物各组分的物质的量不发生变化,据此结合图象判断;
(4)t1时刻后,NO2浓度降低,N2O4浓度增大,未到达平衡状态,反应向正反应进行.
解答 解:(1)可逆反应2NO2?N2O4的平衡常数表达式$K=\frac{{c({N_2}{O_4})}}{{{c^2}{{(N{O_2})}^{\;}}}}$,故答案为:$K=\frac{{c({N_2}{O_4})}}{{{c^2}{{(N{O_2})}^{\;}}}}$;
(2)由图可知,从t1至t2时N2O4的物质的量变化量为4mol-3mol=1mol,故v(N2O4)=$\frac{\frac{1mol}{1L}}{20s-10s}$=0.1mol/(L•s),
故答案为:0.1;
(3)到达平衡时,反应混合物各组分的物质的量不发生变化,由图象可知,t3时刻处于平衡状态,故答案为:t3;
(4)t1时刻后,NO2浓度降低,N2O4浓度增大,未到达平衡状态,反应向正反应进行,故正反应速率大于逆反应速率,
故答案为:>.
点评 本题考查化学平衡图象、化学平衡常数、反应速率计算、化学平衡的影响因素等,难度不大,注意基础知识的理解掌握.

练习册系列答案
相关题目
17.下列叙述正确的是( )
| A. | 固态Na2O2和熔融态NaHSO4中的阴、阳离子个数比均为1:1 | |
| B. | 离子化合物中一定不含共价键 | |
| C. | 某主族元素的最高价含氧酸为HnROm,则其气态氢化物一般是H8-2m+nR或RH8-2m+n | |
| D. | 元素周期表中L层电子为奇数的元素的化合价也都是奇数 |
18.由氧元素的两种同位素16O和18O所形成的两种气体单质18Om和16On,在同温同压同体积时,中子数之比为5:6.则下列有关两种气体的在上述条件下的说法不正确的是( )
| A. | m:n之比为2:3 | B. | 18Om和16On的物质的量比为1:1 | ||
| C. | 18Om和16On的质量比为3:4 | D. | 18Om和16On的密度为2:3 |
2.关于下列各装置图的叙述中,不正确的是( )
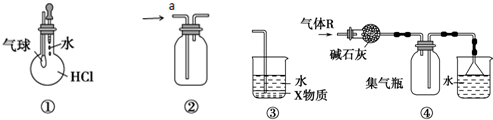

| A. | 装置①可验证HCl气体在水中的溶解性 | |
| B. | 装置②a口进气可用于收集CO2、Cl2或NO等 | |
| C. | 装置③中X为四氯化碳,可用于吸收氨气或氯化氢 | |
| D. | 装置④可用于干燥、收集氨气,并吸收多余的氨气 |
16.能正确表示下列化学反应的离子方程式的是( )
| A. | 氢氧化钡溶液与硫酸的反应 OH-+H+═H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
17.为检验溶液中是否含有Cl-,常采用向溶液中先加HNO3,再加AgNO3溶液的实验方案,若有白色沉淀生成,则证明有Cl-.对此结论,有人提出了质疑,设计了如表探究性实验.
实验一:向Na2SO4溶液中滴加AgNO3溶液
(1)实验一中产生沉淀的离子方程式为2Ag++SO42-═Ag2SO4↓.
(2)学生设计了如表表格,对实验一内容进行理论计算,请帮他完成表格.(表中不要留空格).
25℃时Ksp(Ag2SO4)=1.2×10-5,分析上面数据,若向l mL某溶液中加入3滴0.1mol•L-1 AgNO3溶液,判断下列说法正确的是AD(填字母序号).
A.混合液中c(SO42-)=0.1 mol•L-1 时不会产生Ag2SO4沉淀
B.混合液中c(SO42-)=1 mol•L-1 时不会产生Ag2SO4沉淀
C.无论SO42-浓度大小都会产生Ag2SO4沉淀
D.若使用0.01 mol•L-1 AgNO3溶液,可基本排除SO42-对Cl-检验构成的干扰
(3)某同学在实验一的基础上继续设计了以下实验.
实验二:
已知:H2SO4=H++HSO4-、HSO4-═H++SO42-;对于Ag2SO4溶于硝酸的原因提出了如下假设,请完成假设一.
假设一:H+对Ag2SO4起溶解作用.
假设二:NO3-对Ag2SO4溶解起作用.
(4)从下列限选试剂中选择适当试剂并设计实验方案,分别验证假设一和假设二是否成立.请补齐实验方案(限选试剂:Ag2SO4固体、浓HNO3、NaNO3饱和溶液、CaSO4固体).
①取少量CaSO4固体于试管中,加入一定量浓HNO3,充分振荡.若沉淀溶解,说明假设一成立.
②取少量Ag2SO4固体于试管中,加入一定量NaNO3饱和溶液,充分振荡.若沉淀溶解,说明假设二成立说明假设二成立.
(5)通过(4)的实验发现假设一成立,请用平衡理论解释Ag2SO4溶解的原因Ag2SO4固体在水中存在平衡:Ag2SO4(s)?2Ag+(aq)+SO42-(aq),H+与SO42-结合生成HSO4-,SO42-浓度降低,平衡正向移动,Ag2SO4不断溶解.
结论:该同学组通过实验发现,考虑到Ag+对Cl-检验的灵敏度较高,通常情况下,实验室配制的用来检验Cl-的AgNO3浓度一般较小,所以SO42-对Cl-检验的干扰是完全可以排除的.
实验一:向Na2SO4溶液中滴加AgNO3溶液
| 编号 | Na2SO4溶液 | AgNO3溶液 | 现象 | ||
| 体积/mL | 浓度/(mol•L-1) | 体积 | 浓度/(mol•L-1) | ||
| ① | 1 | 1 | 3滴 | 2 | 出现大量白色沉淀 |
| ② | 1 | 1 | 3滴 | 0.5 | 出现少量白色沉淀 |
| ③ | 1 | 1 | 3滴 | 0.1 | 有些许浑浊 |
| ④ | 1 | 1 | 3滴 | 0.01 | 无明显变化 |
(2)学生设计了如表表格,对实验一内容进行理论计算,请帮他完成表格.(表中不要留空格).
| 编号 | AgNO3浓度/(mol•L-) | 稀释后Ag+浓度/(mol•L-1) | 混合溶液中SO42-的最小理论检出浓度/(mol•L-1) |
| ① | 2 | 0.2 | 0.0003 |
| ② | 0.5 | 0.0048 | |
| ③ | 0.1 | 0.01 | 0.12 |
| ④ | 0.01 | 0.001 |
A.混合液中c(SO42-)=0.1 mol•L-1 时不会产生Ag2SO4沉淀
B.混合液中c(SO42-)=1 mol•L-1 时不会产生Ag2SO4沉淀
C.无论SO42-浓度大小都会产生Ag2SO4沉淀
D.若使用0.01 mol•L-1 AgNO3溶液,可基本排除SO42-对Cl-检验构成的干扰
(3)某同学在实验一的基础上继续设计了以下实验.
实验二:
| 编号 | AgNO3浓度/(mol•L-1) | 现象 | 向沉淀中滴加硝酸后的现象 |
| ① | 2 | 出现大量白色沉淀 | 滴加稀硝酸,沉淀大量溶解;改加浓硝酸,沉淀较快消失 |
| ② | 0.5 | 出现少量白色沉淀 | 滴加稀硝酸,沉淀基本消失 |
假设一:H+对Ag2SO4起溶解作用.
假设二:NO3-对Ag2SO4溶解起作用.
(4)从下列限选试剂中选择适当试剂并设计实验方案,分别验证假设一和假设二是否成立.请补齐实验方案(限选试剂:Ag2SO4固体、浓HNO3、NaNO3饱和溶液、CaSO4固体).
①取少量CaSO4固体于试管中,加入一定量浓HNO3,充分振荡.若沉淀溶解,说明假设一成立.
②取少量Ag2SO4固体于试管中,加入一定量NaNO3饱和溶液,充分振荡.若沉淀溶解,说明假设二成立说明假设二成立.
(5)通过(4)的实验发现假设一成立,请用平衡理论解释Ag2SO4溶解的原因Ag2SO4固体在水中存在平衡:Ag2SO4(s)?2Ag+(aq)+SO42-(aq),H+与SO42-结合生成HSO4-,SO42-浓度降低,平衡正向移动,Ag2SO4不断溶解.
结论:该同学组通过实验发现,考虑到Ag+对Cl-检验的灵敏度较高,通常情况下,实验室配制的用来检验Cl-的AgNO3浓度一般较小,所以SO42-对Cl-检验的干扰是完全可以排除的.