题目内容
5.某溶液经分析,其中只含有Na+、K+、Ca2+、Cl-、NO3-,已知其中Na+、K+、Ca2+、NO3-的浓度均为0.1mol•L-1,则Cl-的物质的量浓度为( )| A. | 0.1mol•L-1 | B. | 0.3mol•L-1 | C. | 0.2mol•L-1 | D. | 0.4mol•L-1 |
分析 离子之间不反应,可共存,且溶液不显电性,结合电荷守恒计算.
解答 解:设Cl-的物质的量浓度为x,Na+、K+、Ca2+、NO3-的浓度均为0.1mol•L-1,
由电荷守恒可知,x+0.1=0.1+0.1+0.1×2,
解得x=0.3mol/L,
故选B.
点评 本题考查物质的量浓度的计算,为高频考点,把握电荷守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法的应用,题目难度不大.

练习册系列答案
相关题目
16.对下列化学反应热现象,不正确的说法是( )
| A. | 放热的反应,不必加热就能发生反应 | |
| B. | 化学反应一定有能量变化 | |
| C. | 化学反应中,吸热反应不一定需要加热也能发生 | |
| D. | 热化学反应方程式中,热效应数值与反应物的物质的量的多少有关 |
13.下列有关物质分类或归纳不正确的是( )
①电解质:明矾、冰醋酸、氯化银、纯碱
②化合物:氯化钡、硝酸、碱石灰、硫酸铜
③混合物:盐酸、漂白粉、水玻璃、水银
④同素异形体:金刚石、石墨、C60.
①电解质:明矾、冰醋酸、氯化银、纯碱
②化合物:氯化钡、硝酸、碱石灰、硫酸铜
③混合物:盐酸、漂白粉、水玻璃、水银
④同素异形体:金刚石、石墨、C60.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
20.继科学家发现C3O2是金星大气成分之后,美国科学家通过“勇气”号太空车探测出水星大气中含有一种称为硫化羰(化学式为COS)的物质,已知硫化羰与二氧化碳的结构相似,但在氧气中会燃烧,下列有关C3O2与硫化羰的说法中不正确的是( )
| A. | 硫化羰在氧气中完全燃烧后的生成物是CO2和SO2 | |
| B. | C3O2与CO一样可以在氧气中燃烧生成CO2 | |
| C. | COS分子中所有原子都满足8电子稳定结构 | |
| D. | CO、C3O2、CO2都是碳的氧化物,它们互为同素异形体 |
10.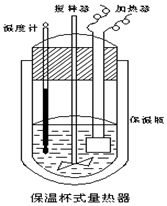 在如图所示的量热计中,将100mL 0.50mol•L-1 CH3COOH 溶液与100mL 0.55mol•L-1NaOH溶液混合,温度从25.0℃升高到27.7℃.已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为 4.184J•g-1•℃-1,两溶液的密度均约为1g•mL-1,下列说法错误的是( )
在如图所示的量热计中,将100mL 0.50mol•L-1 CH3COOH 溶液与100mL 0.55mol•L-1NaOH溶液混合,温度从25.0℃升高到27.7℃.已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为 4.184J•g-1•℃-1,两溶液的密度均约为1g•mL-1,下列说法错误的是( )
 在如图所示的量热计中,将100mL 0.50mol•L-1 CH3COOH 溶液与100mL 0.55mol•L-1NaOH溶液混合,温度从25.0℃升高到27.7℃.已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为 4.184J•g-1•℃-1,两溶液的密度均约为1g•mL-1,下列说法错误的是( )
在如图所示的量热计中,将100mL 0.50mol•L-1 CH3COOH 溶液与100mL 0.55mol•L-1NaOH溶液混合,温度从25.0℃升高到27.7℃.已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为 4.184J•g-1•℃-1,两溶液的密度均约为1g•mL-1,下列说法错误的是( )| A. | 该实验测得的中和热△H为-53.3kJ•mol-1 | |
| B. | 若量热计的保温瓶绝热效果不好,则所测得的△H偏大 | |
| C. | CH3COOH溶液与NaOH溶液的反应为吸热反应 | |
| D. | 所加NaOH溶液过量,目的是保证CH3COOH溶液完全被中和 |
17.某物质 R是人类生命不可缺少的物质.已知 R的摩尔质量为 150g/mol,其中含碳元素 40%,含氢元素 6.7%,其余为氧元素.则 R的化学式为( )
| A. | C5H10O2 | B. | C5H10O5 | C. | C6H6O | D. | C6H12O6 |
14.NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温下7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA | |
| B. | 1mol/L的氯化铁溶液中,若Cl-的数目为3NA,则Fe3+的数目为NA | |
| C. | 反应3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol,当放出热量9.2 kJ时,转移电子0.6 NA | |
| D. | 标准状况下,11.2L三氯甲烷中含有含极性共价键数目为1.5NA |