题目内容
(每空2分,作图3分,共13分)某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为45.3g的该结晶水合物,分别制成溶液。向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24L该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是Al3+和________,阴离子是________。
(2)试通过计算确定:n(Al3+)=________;该结晶水合物的化学式________ 。
(3)假设过程中向该溶液中加入的Ba(OH)2溶液的物质的量浓度为2.0mol/L。
①加入 mLBa(OH)2溶液时,所得沉淀的总物质的量最大。
②请在下图中画出生成沉淀的物质的量与加入Ba(OH)2溶液体积的关系示意图。

(1)NH4+ 、SO42- ;(2) 0.1 mol ; NH4 Al (SO4)2·12H2O [或(NH4)2SO4·Al2(SO4)3·24H2O]
(3)①100
②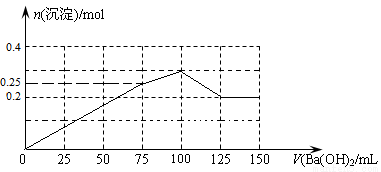
【解析】
试题分析:由于向该溶液中加入NaOH溶液,有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,则该气体是NH3,所以原溶液中含有NH4+,由于加热后共计可收集到2.24L该气体(标准状况),则n(NH4+)=0.1mol;由于向该溶液中加入NaOH溶液,发现溶液中出现白色沉淀并逐渐增多;最后白色沉淀逐渐减少并最终消失,说明含有Al3+;另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g。说明含有SO42-,其物质的量是n(SO42-)= 46.6 g÷233g/mol=0.2mol,则根据电荷守恒可知n(Al3+)=(0.2mol×2-0.1mol×1)÷3=0.1mol,所以n(结晶水)= 45.3g -(0.1mol×18g/mol+0.1mol×27g/mol+0.2mol×96g/mol)=1.2mol,所以n(NH4+):n(Al3+): n(SO42-):n(H2O)=0.1:0.1:0.2:1.2=1:1:2:12,所以该物质的化学式是NH4 Al (SO4)2·12H2O [或(NH4)2SO4·Al2(SO4)3·24H2O];(3)①由于等物质的量的Al(OH)3与BaSO4比较质量BaSO4大,所以沉淀达到最大值时应该是SO42-恰好完全形成沉淀时,n(SO42-)=0.2mol,所以n (Ba(OH)2)= n(SO42-)=0.2mol;V=n÷C=0.2mol÷2.0mol/L=0.1L=100ml; ②向NH4 Al (SO4)2·12H2O的溶液中加入Ba(OH)2溶液,首先发生反应:2NH4 Al (SO4)2+3Ba(OH)2=3BaSO4↓+2Al(OH)3↓+(NH4)2SO4;当该反应完全时,n (Ba(OH)2)=3/2n(NH4 Al (SO4)2)=0.15mol,其体积是V(Ba(OH)2)= 0.15mol÷2mol/L=0.075L=75ml;后再发生反应:(NH4)2SO4+Ba(OH)2=BaSO4↓+2NH3·H2O,由于产生的(NH4)2SO4的物质的量是0.05mol,所以消耗Ba(OH)2的物质的量也是0.05mol,其体积是0.05mol÷2mol/L=0.025L=25ml.继续滴加Ba(OH)2,发生反应Ba(OH)2+2Al(OH)3=Ba(AlO2)2+4H2O.当该反应恰好完全发生时,n(Al(OH)3)=0.1mol,所以消耗Ba(OH)2的物质的量是0.05mol, 其体积是0.05mol÷2mol/L=0.025L=25ml.一共消耗Ba(OH)2的体积是75ml+25ml+25ml=125ml,然后无论如何加入Ba(OH)2,沉淀的质量也不含发生变化,所以图像是:

考点:考查溶液中离子的鉴定、物质化学式的确定、反应产生的沉淀的质量的图像法表示的知识。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO | 稀硫酸 | 3Fe 2++NO |
B | Fe3+、I-、ClO- | 氢氧化钠溶液 | Fe3++3OH-===Fe(OH)3↓ |
C | Ba2+、HCO | 氢氧化钠溶液 | HCO |
D | Al3+、Cl-、NO | 过量氢氧化钠溶液 | Al3++3OH-===Al(OH)3↓ |
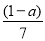 B.
B.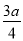 C.
C.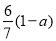 D.
D.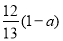
 -C≡C-CH=CH-CH3,有关其结构说法正确的是( )
-C≡C-CH=CH-CH3,有关其结构说法正确的是( )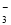 、K+
、K+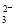 +H2O
+H2O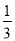 处,手持试管夹长柄末端,进行加热
处,手持试管夹长柄末端,进行加热 CO2(g) + 3H2(g)
CO2(g) + 3H2(g) 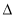 H(298K)=+ 49.4 kJ/mol
H(298K)=+ 49.4 kJ/mol H<0,甲、乙起始反应温度相同,均和外界无热量交换,平衡时,甲中SO2的转化率为a,乙中SO3的分解率为b,则a、b的关系为a+b _______ 1(填“﹤”、“﹥”或“=”) 。
H<0,甲、乙起始反应温度相同,均和外界无热量交换,平衡时,甲中SO2的转化率为a,乙中SO3的分解率为b,则a、b的关系为a+b _______ 1(填“﹤”、“﹥”或“=”) 。