题目内容
8.常温下pH=1的乙酸溶液和pH=13的NaOH溶液,下列叙述中正确的是( )| A. | 乙酸溶液中c(CH3COOH)大于NaOH溶液中c(Na+) | |
| B. | 乙酸溶液中水的电离程度比NaOH溶液中的小 | |
| C. | 若两溶液混合后pH=7,则有:c(Na+)═c(CH3COOH)+c(CH3COO-) | |
| D. | 分别稀释10倍,两溶液的pH之和大于14 |
分析 A.醋酸为弱电解质,在溶液中部分电离出氢离子,氢氧化钠为强电解质,在溶液中完全电离出氢氧根离子;
B.两溶液都抑制了水的电离,乙酸中氢离子与氢氧化钠溶液中的氢氧根离子浓度相等,则抑制程度相同;
C.溶液的pH=7,则c(H+)═c(OH-),根据电荷守恒判断;
D.稀释后醋酸的电离程度增大,则溶液的pH小于2,而稀释后的氢氧化钠溶液的pH=12.
解答 解:A.常温下pH=1的乙酸溶液中氢离子浓度为0.1mol/L,醋酸为弱酸,电离程度减小,醋酸的浓度大于0.1mol/L,pH=13的NaOH溶液中氢氧根离子浓度为0.1mol/L,氢氧化钠为强碱,则氢氧化钠的浓度为0.1mol/L,故乙酸溶液中c(CH3COOH)大于NaOH溶液中c(Na+),故A正确;
B.两溶液都抑制了水的电离,pH=1的乙酸溶液中的氢离子浓度与pH=13的NaOH溶液中氢氧根离子浓度相等,则两溶液对水的电离的影响相同,故B错误;
C.若两溶液混合后pH=7,说明c(H+)═c(OH-),根据电荷守恒可知:c(Na+)═c(CH3COO-),故C错误;
D.分别稀释10倍,醋酸的电离程度增大,则溶液的pH小于2,而稀释后的氢氧化钠溶液的pH=12,则稀释后两溶液的pH之和小于14,故D错误;
故选A.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握电离平衡及其影响、离子浓度大小比较方法,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
18.由氧元素的两种同位素16O和18O所形成的两种气体单质18Om和16On,在同温同压同体积时,中子数之比为5:6.则下列有关两种气体的在上述条件下的说法不正确的是( )
| A. | m:n之比为2:3 | B. | 18Om和16On的物质的量比为1:1 | ||
| C. | 18Om和16On的质量比为3:4 | D. | 18Om和16On的密度为2:3 |
16.能正确表示下列化学反应的离子方程式的是( )
| A. | 氢氧化钡溶液与硫酸的反应 OH-+H+═H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
3.根据表中信息,判断以下叙述正确的是部分短周期元素的原子半径及主要化合价( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的稳定性为H2T<H2R | |
| B. | 单质与稀盐酸反应的剧烈程度为L<Q | |
| C. | R最高价氧化物对应水化物是强酸 | |
| D. | L2+与R2-的核外电子数相等 |
13.如图有关实验装置的说法,不正确的是( )
| A. | 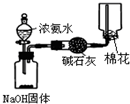 制取收集干燥纯净的NH3 | B. |  称NaOH固体的质量 | ||
| C. | 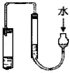 检查此装置的气密性 | D. |  可进行碘水中碘的萃取及分液 |
20.化学已渗透到人类生活的各个方面.下列说法不正确的是( )
| A. | 纤维素在人体内不能被消化吸收,可帮助消化 | |
| B. | 可以用Si3N4、Al2O3制作高温结构陶瓷制品 | |
| C. | 在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀 | |
| D. | 禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染 |
17.为检验溶液中是否含有Cl-,常采用向溶液中先加HNO3,再加AgNO3溶液的实验方案,若有白色沉淀生成,则证明有Cl-.对此结论,有人提出了质疑,设计了如表探究性实验.
实验一:向Na2SO4溶液中滴加AgNO3溶液
(1)实验一中产生沉淀的离子方程式为2Ag++SO42-═Ag2SO4↓.
(2)学生设计了如表表格,对实验一内容进行理论计算,请帮他完成表格.(表中不要留空格).
25℃时Ksp(Ag2SO4)=1.2×10-5,分析上面数据,若向l mL某溶液中加入3滴0.1mol•L-1 AgNO3溶液,判断下列说法正确的是AD(填字母序号).
A.混合液中c(SO42-)=0.1 mol•L-1 时不会产生Ag2SO4沉淀
B.混合液中c(SO42-)=1 mol•L-1 时不会产生Ag2SO4沉淀
C.无论SO42-浓度大小都会产生Ag2SO4沉淀
D.若使用0.01 mol•L-1 AgNO3溶液,可基本排除SO42-对Cl-检验构成的干扰
(3)某同学在实验一的基础上继续设计了以下实验.
实验二:
已知:H2SO4=H++HSO4-、HSO4-═H++SO42-;对于Ag2SO4溶于硝酸的原因提出了如下假设,请完成假设一.
假设一:H+对Ag2SO4起溶解作用.
假设二:NO3-对Ag2SO4溶解起作用.
(4)从下列限选试剂中选择适当试剂并设计实验方案,分别验证假设一和假设二是否成立.请补齐实验方案(限选试剂:Ag2SO4固体、浓HNO3、NaNO3饱和溶液、CaSO4固体).
①取少量CaSO4固体于试管中,加入一定量浓HNO3,充分振荡.若沉淀溶解,说明假设一成立.
②取少量Ag2SO4固体于试管中,加入一定量NaNO3饱和溶液,充分振荡.若沉淀溶解,说明假设二成立说明假设二成立.
(5)通过(4)的实验发现假设一成立,请用平衡理论解释Ag2SO4溶解的原因Ag2SO4固体在水中存在平衡:Ag2SO4(s)?2Ag+(aq)+SO42-(aq),H+与SO42-结合生成HSO4-,SO42-浓度降低,平衡正向移动,Ag2SO4不断溶解.
结论:该同学组通过实验发现,考虑到Ag+对Cl-检验的灵敏度较高,通常情况下,实验室配制的用来检验Cl-的AgNO3浓度一般较小,所以SO42-对Cl-检验的干扰是完全可以排除的.
实验一:向Na2SO4溶液中滴加AgNO3溶液
| 编号 | Na2SO4溶液 | AgNO3溶液 | 现象 | ||
| 体积/mL | 浓度/(mol•L-1) | 体积 | 浓度/(mol•L-1) | ||
| ① | 1 | 1 | 3滴 | 2 | 出现大量白色沉淀 |
| ② | 1 | 1 | 3滴 | 0.5 | 出现少量白色沉淀 |
| ③ | 1 | 1 | 3滴 | 0.1 | 有些许浑浊 |
| ④ | 1 | 1 | 3滴 | 0.01 | 无明显变化 |
(2)学生设计了如表表格,对实验一内容进行理论计算,请帮他完成表格.(表中不要留空格).
| 编号 | AgNO3浓度/(mol•L-) | 稀释后Ag+浓度/(mol•L-1) | 混合溶液中SO42-的最小理论检出浓度/(mol•L-1) |
| ① | 2 | 0.2 | 0.0003 |
| ② | 0.5 | 0.0048 | |
| ③ | 0.1 | 0.01 | 0.12 |
| ④ | 0.01 | 0.001 |
A.混合液中c(SO42-)=0.1 mol•L-1 时不会产生Ag2SO4沉淀
B.混合液中c(SO42-)=1 mol•L-1 时不会产生Ag2SO4沉淀
C.无论SO42-浓度大小都会产生Ag2SO4沉淀
D.若使用0.01 mol•L-1 AgNO3溶液,可基本排除SO42-对Cl-检验构成的干扰
(3)某同学在实验一的基础上继续设计了以下实验.
实验二:
| 编号 | AgNO3浓度/(mol•L-1) | 现象 | 向沉淀中滴加硝酸后的现象 |
| ① | 2 | 出现大量白色沉淀 | 滴加稀硝酸,沉淀大量溶解;改加浓硝酸,沉淀较快消失 |
| ② | 0.5 | 出现少量白色沉淀 | 滴加稀硝酸,沉淀基本消失 |
假设一:H+对Ag2SO4起溶解作用.
假设二:NO3-对Ag2SO4溶解起作用.
(4)从下列限选试剂中选择适当试剂并设计实验方案,分别验证假设一和假设二是否成立.请补齐实验方案(限选试剂:Ag2SO4固体、浓HNO3、NaNO3饱和溶液、CaSO4固体).
①取少量CaSO4固体于试管中,加入一定量浓HNO3,充分振荡.若沉淀溶解,说明假设一成立.
②取少量Ag2SO4固体于试管中,加入一定量NaNO3饱和溶液,充分振荡.若沉淀溶解,说明假设二成立说明假设二成立.
(5)通过(4)的实验发现假设一成立,请用平衡理论解释Ag2SO4溶解的原因Ag2SO4固体在水中存在平衡:Ag2SO4(s)?2Ag+(aq)+SO42-(aq),H+与SO42-结合生成HSO4-,SO42-浓度降低,平衡正向移动,Ag2SO4不断溶解.
结论:该同学组通过实验发现,考虑到Ag+对Cl-检验的灵敏度较高,通常情况下,实验室配制的用来检验Cl-的AgNO3浓度一般较小,所以SO42-对Cl-检验的干扰是完全可以排除的.