题目内容
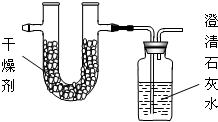 营养学研究发现,从深海鱼油提取的DHA是一种不饱和高级脂肪酸(假设DHA的化学式为CxHyO2),同温同压条件下,测得DHA蒸汽的质量是同体积H2质量的192倍;将3.84g的DHA完全燃烧,并使产生的产物全部依次通过如图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).
营养学研究发现,从深海鱼油提取的DHA是一种不饱和高级脂肪酸(假设DHA的化学式为CxHyO2),同温同压条件下,测得DHA蒸汽的质量是同体积H2质量的192倍;将3.84g的DHA完全燃烧,并使产生的产物全部依次通过如图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).| 实验前 | 实验后 | (干燥剂+U型管)的质量 | 101.1g | 104.70g | (石灰水+广口瓶)的质量 | 312.0g | 323.44g |
(2)另取DHA和足量的溴水反应,发现3.84gDHA可以和0.06mol的溴发生加成反应,问一个DHA分子中含有多少个碳碳双键?
分析:(1)根据相对密度之比等于相对分子质量之比计算该烃的相对分子质量,进而计算3.84g该烃燃烧生成水和二氧化碳的质量,可计算化学式;
(2)根据1个C=C能与1个溴分子加成,据此判断.
(2)根据1个C=C能与1个溴分子加成,据此判断.
解答:解:(1)由n=
=
可知相对密度之比等于相对分子质量之比,确定该烃的相对分子质量为2×192=384,
所以3.84g该烃的物质的量为
=0.01mol,
由表中数据可知,干燥管增重的质量为水的质量,则n(H2O)=
=0.2mol,n(H)=0.4mol,
广口瓶增重的质量为二氧化碳的质量,则n(CO2)=
=0.26mol,
则1mol烃中含有
=40molH原子,含有
=26molC原子,
所以分子式为C26H40O2,
答:DHA的相对分子质量为384,化学式为C26H40O2;
(2)另取DHA和足量的溴水反应,发现3.84g即0.01molDHA可以和0.06mol的溴发生加成反应,则DHA与溴的物质的量之比为1:6,已知molC=C能与mol溴分子加成,所以一个DHA分子中含6个C=C;
答:一个DHA分子中含6个C=C.
| m |
| M |
| V |
| Vm |
所以3.84g该烃的物质的量为
| 3.84g |
| 384g/mol |
由表中数据可知,干燥管增重的质量为水的质量,则n(H2O)=
| 104.70g-101.1g |
| 18g/mol |
广口瓶增重的质量为二氧化碳的质量,则n(CO2)=
| 323.44g-312.0g |
| 44g/mol |
则1mol烃中含有
| 0.4mol |
| 0.01 |
| 0.26mol |
| 0.01 |
所以分子式为C26H40O2,
答:DHA的相对分子质量为384,化学式为C26H40O2;
(2)另取DHA和足量的溴水反应,发现3.84g即0.01molDHA可以和0.06mol的溴发生加成反应,则DHA与溴的物质的量之比为1:6,已知molC=C能与mol溴分子加成,所以一个DHA分子中含6个C=C;
答:一个DHA分子中含6个C=C.
点评:本题考查有机物分子式的确定,题目难度不大,注意有机物与溴加成时C=C与溴的关系.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
营养学研究发现,从深海鱼油提取的DHA是一种不饱和高级脂肪酸(假设DHA的化学式为CxHyO2),同温同压条件下,测得DHA蒸汽的质量是同体积H2质量的192倍;将3.84g的DHA完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收)。
| 实验前 | 实验后 |
(干燥剂+U型管)的质量 | 101.1g | 104.70g |
(石灰水+广口瓶)的质量 | 312.0g | 323.44g |
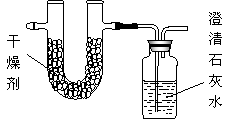
(1)根据上表数据确定DHA的相对分子质量和化学式;(写出计算过程)
(2)另取DHA和足量的溴水反应,发现3.84gDHA可以和0.06mol的溴发生加成反应,问一个DHA分子中含有多少个C=C?
营养学研究发现,从深海鱼油提取的DHA是一种不饱和高级脂肪酸(假设DHA的化学式为CxHyO2),同温同压条件下,测得DHA蒸汽的质量是同体积H2质量的192倍;将3.84g的DHA完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收)。
| 实验前 | 实验后 | |
| (干燥剂+U型管)的质量 | 101.1g | 104.70g |
| (石灰水+广口瓶)的质量 | 312.0g | 323.44g |
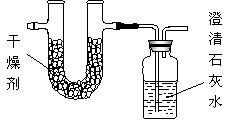
(1)根据上表数据确定DHA的相对分子质量和化学式;(写出计算过程)
(2)另取DHA和足量的溴水反应,发现3.84gDHA可以和0.06mol的溴发生加成反应,问一个DHA分子中含有多少个C=C?
.
 营养学研究发现,从深海鱼油提取的DHA是一种不饱和高级脂肪酸(假设DHA的化学式为CxHyO2),同温同压条件下,测得DHA蒸汽的质量是同体积H2质量的192倍;将3.84g的DHA完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).
营养学研究发现,从深海鱼油提取的DHA是一种不饱和高级脂肪酸(假设DHA的化学式为CxHyO2),同温同压条件下,测得DHA蒸汽的质量是同体积H2质量的192倍;将3.84g的DHA完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).
