题目内容
13g锌与100g稀硫酸恰好完全反应,求所得溶液中溶质的质量分数.(计算结果精确到0.1%)
考点:化学方程式的有关计算
专题:计算题
分析:发生反应:Zn+H2SO4═ZnSO 4+H 2↑,根据方程式计算硫酸锌的质量、生成氢气的质量,进而计算溶液质量,再根据质量分数定义计算.
解答:
解:设生成ZnSO4的质量为x,生成H2的质量为y,则:
Zn+H2SO4═ZnSO4+H2↑
65 161 2
13 g x y
x=
=32.2g
y=
=0.4g
所得溶液质量=13g+100g-0.4g=112.6g
所得溶液中溶质的质量分数为:
×100%=28.6%
答:所得溶液中溶质的质量分数为28.6%.
Zn+H2SO4═ZnSO4+H2↑
65 161 2
13 g x y
x=
| 13g×161 |
| 65 |
y=
| 13g×2 |
| 65 |
所得溶液质量=13g+100g-0.4g=112.6g
所得溶液中溶质的质量分数为:
| 32.2g |
| 112.6g |
答:所得溶液中溶质的质量分数为28.6%.
点评:本题考查化学方程式计算、溶液质量分数计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
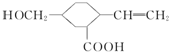 某有机物的结构如图所示,下列各项性质中,它不可能具有的是( )
某有机物的结构如图所示,下列各项性质中,它不可能具有的是( )①可以燃烧
②能使酸性高锰酸钾溶液褪色
③能跟NaOH溶液反应
④能发生酯化反应
⑤能发生聚合反应
⑥能发生水解反应
⑦能发生取代反应.
| A、⑥ | B、①④ | C、⑤ | D、④⑥ |
两种气态烷烃的混合物,在标准状况下其密度为1.03g?L-1,则关于该混合物组成的说法正确的是( )
| A、一定有甲烷 |
| B、一定有乙烷 |
| C、不可能是甲烷和乙烷的混合物 |
| D、可能是乙烷和丙烷的混合物 |
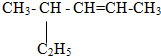
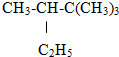
 用锌片与稀硫酸反应,实验结果记录如表
用锌片与稀硫酸反应,实验结果记录如表