题目内容
14.现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子.请回答下列问题:
(1)E、F气态氢化物的稳定性为HCl>H2S(用化学式表示).
(2)E与F可形成E2F2的化合物,其电子式为
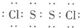 ,其晶体类型为分子晶体.
,其晶体类型为分子晶体.(3)C、D形成的一种化合物能与D、E形成的化合物在溶液中发生氧化还原反应,其离子方程式为:Na2O2+S2-+2H2O=S↓+2Na++4OH-.
(4)A、C、E三种元素形成的一种常见化合物H,其浓溶液在加热条件下可与a g铜反应,则被还原的H的物质的量为$\frac{a}{64}$mol.
(5)E的一种常见氧化物为大气污染物,实验室可用足量D的最高价氧化物的水化物来吸收,则吸收生成的盐溶液中离子浓度大小关系为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
(6)b g D单质在纯净的C单质中燃烧放出Q kJ热量,则相关的热化学方程式为:2Na(s)+O2(g)=Na2O2(s)△H=-$\frac{46Q}{b}$kJ/mol.
分析 A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与C形成的化合物常温下为液态,则A为H元素,C为O元素;A、B的最外层电子数之和与C的最外层电子数相等,B的最外层电子数为5,则B为N元素;A、D同主族,则D为Na元素;C与E同主族,则E为S元素;D、E、F同周期,A能分别与E、F形成电子总数相等的气体分子,则F为Cl元素.
(1)非金属性越强,对应氢化物越稳定;
(2)E2F2为S2Cl2,以共价键形成的分子,为分子晶体;
(3)C、D形成的一种化合物为Na2O2,具有强氧化性,D、E形成的化合物为Na2S,在溶液中反应生成氢氧化钠与硫;
(4)化合物H为硫酸,由电子守恒来计算;
(5)二氧化硫与足量的NaOH溶液吸收生成亚硫酸钠,溶液中亚硫酸根离子水解,溶液呈碱性,溶液中氢氧根离子源于水的电离、亚硫酸根及亚硫酸氢根离子水解;
(6)发生反应:2Na+O2=Na2O2,计算2molNa反应放出的热量,注明物质的聚集状态与反应热书写热化学方程式.
解答 解:A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与C形成的化合物常温下为液态,则A为H元素,C为O元素;A、B的最外层电子数之和与C的最外层电子数相等,B的最外层电子数为5,则B为N元素;A、D同主族,则D为Na元素;C与E同主族,则E为S元素;D、E、F同周期,A能分别与E、F形成电子总数相等的气体分子,则F为Cl元素.
(1)非金属性Cl>S,则气态氢化物的稳定为HCl>H2S,故答案为:HCl;H2S;
(2)E2F2为S2Cl2,以共价键形成的分子,其电子式为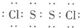 ,构成微粒为分子,则为分子晶体,故答案为:
,构成微粒为分子,则为分子晶体,故答案为: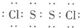 ;分子晶体;
;分子晶体;
(3)C、D形成的一种化合物为Na2O2,具有强氧化性,D、E形成的化合物为Na2S,二者发生氧化还原反应,其离子反应为Na2O2+S2-+2H2O=S↓+2Na++4OH-,
故答案为:Na2O2+S2-+2H2O=S↓+2Na++4OH-;
(4)化合物H为硫酸,Cu与浓硫酸反应中Cu失去电子,S得到电子,设S的物质的量为x,由电子守恒可知,x×(6-4)=$\frac{ag}{64g/mol}$×(2-0),解得x=$\frac{a}{64}$mol,
故答案为:$\frac{a}{64}$mol;
(5)二氧化硫与足量的NaOH溶液吸收生成亚硫酸钠,溶液中亚硫酸根离子水解,溶液呈碱性,溶液中氢氧根离子源于水的电离、亚硫酸根及亚硫酸氢根离子水解,则离子的浓度为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+),
故答案为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+);
(6)bgNa燃烧生成过氧化钠放出的热量为QkJ,则46gNa燃烧放出的热量为$\frac{46Q}{b}$kJ,则热化学反应方程式为2Na(s)+O2(g)=Na2O2(s)△H=-$\frac{46Q}{b}$kJ/mol,
故答案为:2Na(s)+O2(g)=Na2O2(s)△H=-$\frac{46Q}{b}$kJ/mol.
点评 本题考查位置结构性质的关系及应用,综合性较强,考查知识点较多,元素的推断是解答本题的关键,并熟悉元素化合物的性质,难度中等.

(1)煤的气化:用化学方程式表示出煤的气化的主要反应C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2:
(2)煤的液化:下表中有些反应是煤液化过程中的反应:
| 热化学方程式 | 平衡常数 | |
| 500℃ | 700℃ | |
| ①2H2(g)+CO(g)?CH3OH(g)△H1=a kJ•mol-1 | 2.5 | 0.2 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g)△H2=b kJ•mol-1 | 1.0 | 2.3 |
| ③3H2(g)+CO2 (g)?CH3OH(g)+H2O(g)△H3=c kJ•mol-1 | K3 | 4.6 |
②K3=2.5,若反应③是在容积为2L的密闭容器巾进行(500℃)的,测得某一时刻体系内H2、CO2、CH3OH、H2O物质的量分别为6mol、2mol、10mol、10mol,则此时CH3OH的生成速率>(填“>”、“<”、“=”) CH3OH的消耗速率.
(3)烯烃化阶段:如图l是某工厂烯烃化阶段产物中乙烯、丙烯的选择性与温度、压强之间的关系(选择性:指生成某物质的百分比,图中I、Ⅱ表示乙烯,Ⅲ表示丙烯).
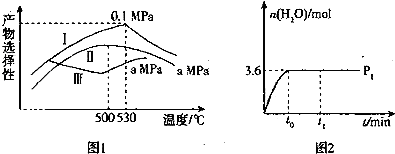
①尽可能多地获得乙烯,控制的生产条件为530℃,0.1Mpa.
②一定温度下某密闭容器中存在反应,2CH3OH(g)?CH2=CH2(g)+2H2O(g)△H>0.在压强为P1时,产物水的物质的量与时间的关系如图2所示,若t0 时刻,测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为85.7%(保留三位有效数字),若在t1 时刻将容器容积快速扩大到原来的2倍,请在图中绘制出此变化发生后至反应达到新平衡时水的物质的量与时间的关系图.
| 试剂 | 离子反应方程式 | |
| ①Fe(Al) | ||
| ②FeCl 2溶液(FeCl3) |
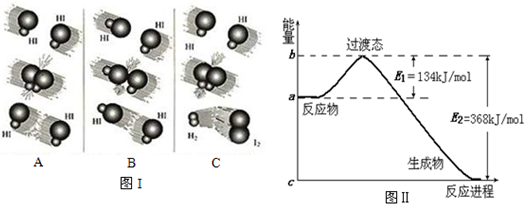
(1)图Ⅰ是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是C(选填“A”、“B”或“C”);
(2)图Ⅱ是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,则写出该反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234 kJ/mol
(3)E1的大小对该反应的反应热有无影响?无.(选填“有”或“无”)
(4)进一步研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1mol化学键时所需吸收的能量.如表是部分化学键的键能数据:
| 化学键 | C-H | Cl-Cl | C-Cl | H-Cl |
| 键能/kJ•mol-1 | X | 243 | 330 | 432 |
(5)已知:①C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol-1
②2CO(g)+O2(g)═2CO2(g);△H=-566kJ•mol-1
③TiO2(s)+2Cl2(g)═TiCl4(s)+O2(g);△H=+141kJ•mol-1
则TiO2(s)+2Cl2(g)+2C(s)═TiCl4(s)+2CO(g)的△H=-80KJ/mol.
| A. | 减小C和D的浓度 | B. | 增大D的浓度 | C. | 减小B的浓度 | D. | 增大A和B的浓度 |
| A. | 跟水反应时,水作氧化剂 | |
| B. | NaH中阳离子半径大于阴离子半径 | |
| C. | 跟液氨反应时,生成氢气外,还生成铵盐 | |
| D. | 与乙醇反应时,放出氢气的速率比与水反应时更快 |
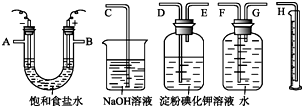 请用如图所示仪器设计一个电解饱和食盐水并测定电解时产生的H2的体积和检验Cl2的实验装置.(提示:Cl2可与KI反应生成I2,淀粉遇I2变蓝)
请用如图所示仪器设计一个电解饱和食盐水并测定电解时产生的H2的体积和检验Cl2的实验装置.(提示:Cl2可与KI反应生成I2,淀粉遇I2变蓝)