题目内容
设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A、标准状况下,0.5 mol SO3中含有1.5NA个O原子 |
| B、常温常压下,22 g 14CO2中所含分子数为0.5NA |
| C、室温下,1 L pH=1的H2SO4溶液中含有的H+数目为0.2NA |
| D、7.8g Na2O2与足量水反应,转移电子数为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.1mol SO3中含有1.5molO原子;
B.14CO2的摩尔质量是46g/mol;
C.pH计算氢离子浓度,依据n=cV计算溶质物质的量;
D.根据过氧化钠的物质的量和O元素的化合价分析.
B.14CO2的摩尔质量是46g/mol;
C.pH计算氢离子浓度,依据n=cV计算溶质物质的量;
D.根据过氧化钠的物质的量和O元素的化合价分析.
解答:
解:A.1mol SO3中含有1.5molO原子,0.5 mol SO3中含有1.5NA个O原子,故A正确;
B.14CO2的摩尔质量是46g/mol,22 g 14CO2的物质的量不是0.5mol,故B错误;
C.pH=1的溶液中c(H+)=0.1mol/L,1.0 L H2SO4溶液中含有的H+的数目为0.1NA,故C错误;
D.7.8g过氧化钠为0.1mol,与足量水反应,自身发生氧化还原反应,转移电子数为0.1NA,故D错误.
故选A.
B.14CO2的摩尔质量是46g/mol,22 g 14CO2的物质的量不是0.5mol,故B错误;
C.pH=1的溶液中c(H+)=0.1mol/L,1.0 L H2SO4溶液中含有的H+的数目为0.1NA,故C错误;
D.7.8g过氧化钠为0.1mol,与足量水反应,自身发生氧化还原反应,转移电子数为0.1NA,故D错误.
故选A.
点评:本题考查阿伏加德罗常数的相关计算,题目难度不大,注意物质的组成、结构、性质以及物质存在的外界条件和聚集状态等问题.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
下列叙述正确的是( )
| A、乙酸所有原子处于同一平面,含有羧基,可与NaHCO3溶液反应生成CO2 |
| B、苯、乙醇和乙酸都能发生取代反应,乙酸乙酯和食用植物油均可水解生成乙醇 |
| C、乙烯、苯和聚乙烯都能使溴水褪色,褪色的原因相同 |
| D、在烃类有机物分子中,含有的氢原子个数一定是偶数 |
下列说法不正确的是( )
| A、工业上冶炼Fe用热还原方法 |
| B、海水淡化的方法主要有蒸馏法,电渗析法,离子交换法等 |
| C、工业上通过煤的干馏可获得芳香烃 |
| D、单质硅是将太阳能转变为电能的材料,二氧化硅可以做半导体材料 |
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A、X与Y形成化合物,X可以显负价,Y显正价 |
| B、第一电离能可能Y小于X |
| C、气态氢化物的稳定性:HmY小于HnX |
| D、最高价含氧酸的酸性:X对应的酸性弱于于Y对应的 |
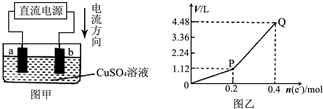 用惰性电极电解一定量的硫酸铜溶液,实验装置如图甲.电解过程中的实验数据如图乙,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).则下列说法不正确的是( )
用惰性电极电解一定量的硫酸铜溶液,实验装置如图甲.电解过程中的实验数据如图乙,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).则下列说法不正确的是( )| A、电解过程中,a电极表面先有红色物质析出,后有气泡产生 |
| B、b电极上发生的反应方程式为:4OH--4e-=2H2O+O2↑ |
| C、曲线0~P段表示O2的体积变化 |
| D、从开始到Q点时收集到的混合气体的平均摩尔质量为12g?mol-1 |
用NA表示阿伏加德罗常数,下列判断正确的是( )
| A、常温常压下,16g O2和O3的混合气体中含有NA个氧原子 |
| B、常温常压下,28 g CO与22.4 L O2的分子数都是NA个 |
| C、16 g CH4与18 g NH4+所含质子数都是10NA个 |
| D、1 mol/L Na2CO3溶液中,CO32-的离子数目小于NA个 |
化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是( )
①加快化石燃料的开采与使用;
②研发易降解的生物农药;
③应用高效洁净的能源转换技术;
④田间焚烧秸秆;
⑤酶催化反应具有高效、专一、条件温和等特点,化学模拟生物酶对绿色化学、环境保护及节能减排具有重要意义.
①加快化石燃料的开采与使用;
②研发易降解的生物农药;
③应用高效洁净的能源转换技术;
④田间焚烧秸秆;
⑤酶催化反应具有高效、专一、条件温和等特点,化学模拟生物酶对绿色化学、环境保护及节能减排具有重要意义.
| A、①③⑤ | B、②③⑤ |
| C、①②④ | D、②④⑤ |
有人认为CH2=CH2与Br2的加成反应,实质是Br2先断裂为Br+和Br-,然后Br+首先与CH2=CH2一端碳原子结合,第二步才是Br-与另一端碳原子结合.根据该观点如果让CH2=CH2与Br2在盛有NaCl和NaI的水溶液中反应,则得到的有机物是( )
| A、ICH2CH2I |
| B、ClCH2CH2Br |
| C、ClCH2CH2I |
| D、ClCH2CH2Cl |