题目内容
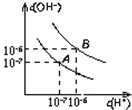 已知水在25℃和100℃时,其电离平衡曲线如图所示:
已知水在25℃和100℃时,其电离平衡曲线如图所示:(1)25℃时水的电离平衡曲线应为
(2)100℃时,将pH=12的NaOH溶液与pH=3的H2SO4溶液混合,若所得混合溶液的pH=6,则NaOH溶液与H2SO4溶液的体积比为
(3)25℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是
(4)曲线B对应温度下,pH=3的盐酸溶液和pH=9的某碱溶液等体积混合后,混合溶液的pH=7.请分析原因:
考点:水的电离,pH的简单计算,酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:(1)水的电离是吸热过程,降低温度抑制水电离,导致水中c(H+)、c(OH-)都减小;
(2)100℃时,若所得混合溶液的pH=6,说明两者恰好完全反应溶液呈中性;
(3)混合溶液呈中性,说明酸中氢离子的物质的量等于碱中氢氧根离子的物质的量;
(4)pH=3的盐酸溶液和pH=9的某碱溶液等体积混合后,氢离子和氢氧根离子恰好反应,根据盐的性质分析.
(2)100℃时,若所得混合溶液的pH=6,说明两者恰好完全反应溶液呈中性;
(3)混合溶液呈中性,说明酸中氢离子的物质的量等于碱中氢氧根离子的物质的量;
(4)pH=3的盐酸溶液和pH=9的某碱溶液等体积混合后,氢离子和氢氧根离子恰好反应,根据盐的性质分析.
解答:
解:(1)水的电离是吸热过程,升高温度,使水的电离程度增大,当温度升高时,促进水的电离,水的离子积增大,水中氢离子、氢氧根离子浓度都增大,水的pH减小,但溶液仍然呈中性;故答案为:A;水的电离是吸热过程,温度低时,电离程度小,c(H+)、c(OH-)小;
(2)将pH=12的NaOH溶液,氢氧离子的浓度为1mol/l与pH=3的H2SO4溶液氢离子的浓度为10-3mol/l混合,溶液呈中则氢离子与氢氧根离子的物质的量相等,所以1mol/l×Vb=10-3mol/l×Va,则NaOH溶液与H2SO4溶液的体积比为1:1000,故答案为:1:1000;
(3)25℃时,若100体积pH1=a的某强酸溶液中氢离子的物质的量浓度=10-a mol/L,1体积pH2=b的某强碱溶液中氢氧根离子的物质的量浓度=10 b-14mol/L,混合后溶液呈中性,则氢离子的物质的量等于氢氧根离子的物质的量,所以100×10-a mol/L=1×10 b-14 mol/L,所以a+b=16(或pH1+pH2═16)
故答案为:a+b=16(或pH1+pH2═16);
(4)100℃时,pH=3的盐酸溶液和pH=9的某碱溶液等体积混合后,氢离子和氢氧根离子恰好反应,如果碱是强碱,则盐溶液呈中性,实际上溶液呈碱性,则碱为弱碱,生成强酸弱碱盐水解呈碱性,故答案为:该碱为弱碱.
(2)将pH=12的NaOH溶液,氢氧离子的浓度为1mol/l与pH=3的H2SO4溶液氢离子的浓度为10-3mol/l混合,溶液呈中则氢离子与氢氧根离子的物质的量相等,所以1mol/l×Vb=10-3mol/l×Va,则NaOH溶液与H2SO4溶液的体积比为1:1000,故答案为:1:1000;
(3)25℃时,若100体积pH1=a的某强酸溶液中氢离子的物质的量浓度=10-a mol/L,1体积pH2=b的某强碱溶液中氢氧根离子的物质的量浓度=10 b-14mol/L,混合后溶液呈中性,则氢离子的物质的量等于氢氧根离子的物质的量,所以100×10-a mol/L=1×10 b-14 mol/L,所以a+b=16(或pH1+pH2═16)
故答案为:a+b=16(或pH1+pH2═16);
(4)100℃时,pH=3的盐酸溶液和pH=9的某碱溶液等体积混合后,氢离子和氢氧根离子恰好反应,如果碱是强碱,则盐溶液呈中性,实际上溶液呈碱性,则碱为弱碱,生成强酸弱碱盐水解呈碱性,故答案为:该碱为弱碱.
点评:本题考查了离子积常数的有关计算,注意碱溶液中氢氧根离子浓度的计算方法,为易错点.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
萤火虫会在夏日的夜空发出点点光亮,这是一种最高效的发光机制.萤火虫发光的原理是荧光素在荧光酶和ATP催化下发生氧化还原反应时伴随着化学能转变为光能:

荧光素属于( )

荧光素属于( )
| A、烃的衍生物 | B、高分子化合物 |
| C、无机物 | D、烃 |
10月21日哈尔滨出现了严重的雾霾天气,致使高速公路关闭,航班停飞.雾霾属于下列分散系中的( )
| A、溶液 | B、悬浊液 |
| C、乳浊液 | D、胶体 |
下列有机物的名称正确的是( )
| A、2-乙基-3,3-二甲基-4-乙基戊烷 |
| B、3,3,4-三甲基已烷 |
| C、3,3-二甲基-4-乙基戊烷 |
| D、2-甲基-3-丁烯 |
