题目内容
下列说法中正确的是( )
| A、HCHO分子中既含σ键又含π键 |
| B、CO2分子中的化学键为非极性键 |
| C、NH3分子中N原子的杂化轨道类型是sp2 |
| D、沸点:HF>NH3>H2O |
考点:共价键的形成及共价键的主要类型,极性键和非极性键,原子轨道杂化方式及杂化类型判断,氢键的存在对物质性质的影响
专题:
分析:A.单键含有一个δ键,双键含有一个δ键和一个π键,结合甲醛的结构式分析;
B.不同非金属原子之间形成极性键;
C.根据中心原子的价层电子对数判断;
D.含有氢键的氢化物,氢键数目越多,沸点越高,元素的非金属越强,越易形成氢键,其沸点越高.
B.不同非金属原子之间形成极性键;
C.根据中心原子的价层电子对数判断;
D.含有氢键的氢化物,氢键数目越多,沸点越高,元素的非金属越强,越易形成氢键,其沸点越高.
解答:
解:A.单键含有一个δ键,双键含有一个δ键和一个π键,已知甲醛的结构简式为H-
-H,则分子中既含σ键又含π键,故A正确;
B.不同非金属原子之间形成极性键,则CO2分子中C与O形成极性键,故B错误;
C.NH3分子中N原子的价层电子对数为3+
(5-3×1)=4,sp3为杂化,故C错误;
D.含有氢键的氢化物,氢键数目越多,沸点越高,元素的非金属越强,越易形成氢键,其沸点越高,则沸点:H2O>HF>NH3,故D错误;
故选A.
| ||
| C |
B.不同非金属原子之间形成极性键,则CO2分子中C与O形成极性键,故B错误;
C.NH3分子中N原子的价层电子对数为3+
| 1 |
| 2 |
D.含有氢键的氢化物,氢键数目越多,沸点越高,元素的非金属越强,越易形成氢键,其沸点越高,则沸点:H2O>HF>NH3,故D错误;
故选A.
点评:本题考查了共价键、杂化类型的判断、氢键等,题目难度不大,侧重于基础知识的考查,注意把握杂化轨道理论及其应用.

练习册系列答案
相关题目
下列关于氧化还原反应实质的说法中,比较确切的是( )
| A、有电子转移 |
| B、有电子得失 |
| C、得氧或失氧 |
| D、有元素化合价变化 |
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子.根据以上叙述,下列说中正确的是( )
| A、W、X、Y、Z原子的核外最外层电子数的总和为20 |
| B、上述W、X、Y元素的原子半径大小为W<X<Y |
| C、由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
| D、W与Y可形成既含极性共价键又含非极性共价键的化合物 |
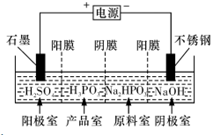 亚磷酸(H3P03 )是二元酸,H3 P03溶液中存在电离平衡:H3PO3?H-+H2PO3-亚磷酸与足量NaOH溶液反应,生成Na2 HPO3.
亚磷酸(H3P03 )是二元酸,H3 P03溶液中存在电离平衡:H3PO3?H-+H2PO3-亚磷酸与足量NaOH溶液反应,生成Na2 HPO3.