题目内容
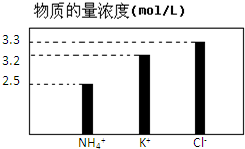 在无土栽培中,需配置20L含NH4Cl、KCl和K2CO3的营养液.营养液中部分离子的物质的量浓度如图所示.若用KCl、NH4Cl和(NH4)2CO3三种固体为原料来配制上述营养液,则需KCl、NH4Cl和(NH4)2CO3三种固体得物质的量依次为(单位为mol)( )
在无土栽培中,需配置20L含NH4Cl、KCl和K2CO3的营养液.营养液中部分离子的物质的量浓度如图所示.若用KCl、NH4Cl和(NH4)2CO3三种固体为原料来配制上述营养液,则需KCl、NH4Cl和(NH4)2CO3三种固体得物质的量依次为(单位为mol)( )| A、2、64、24 |
| B、16、50、24 |
| C、32、50、12 |
| D、64、2、24 |
考点:电解质在水溶液中的电离,物质的量浓度的相关计算
专题:离子反应专题
分析:本题可以根据离子守恒的思想来解决,已知溶液的体积为20L,则n(NH4+)=2.5mol/L×20L=50mol,n(K+)=3.2mol/L×20L=64mol,n(Cl-)=3.3mol/L×20L=66mol,根据只有KCl可以提供钾离子,64mol KCl中钾离子为64mol作为解题的入手点.
解答:
解:需配置20L含NH4Cl、KCl和K2CO3的营养液,营养液中离子的物质的量分别为:n(NH4+)=2.5mol/L×20L=50mol,n(K+)=3.2mol/L×20L=64mol,n(Cl-)=3.3mol/L×20L=66mol,
根据只有KCl可以提供钾离子,64mol KCl中钾离子为64mol,
由氯离子守恒得n(NH4Cl)=66mol-64mol×2=2mol,
再由铵根离子守恒,则n[(NH4)2CO3]=
(50mol-2mol)=24mol,
故选D.
根据只有KCl可以提供钾离子,64mol KCl中钾离子为64mol,
由氯离子守恒得n(NH4Cl)=66mol-64mol×2=2mol,
再由铵根离子守恒,则n[(NH4)2CO3]=
| 1 |
| 2 |
故选D.
点评:本题考查了物质的量的有关计算,考查学生守恒思想在解题中的应用,要求学生具有一定的分析和解决问题的能力,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A、原子半径:X>W>Y |
| B、Y、Z的阴离子电子层结构都与R原子的相同 |
| C、W的氢化物比X的氢化物稳定 |
| D、Y元素的最高价氧化物对应水化物比W元素的最高价氧化物对应水化物的酸性强 |
下面是四位同学对“化学与健康”这一话题发表的见解,正确的是( )
| A、多食用海产品可防治缺铁性贫血 |
| B、食物可调节人体细胞中的酸碱平衡 |
| C、为了减肥,我每天只吃水果、蔬菜 |
| D、我国应该禁止使用食物防腐剂 |
下列叙述正确的是( )
| A、向0.1 mol/L醋酸溶液中加入少量醋酸钠溶液,溶液的pH增大 |
| B、向0.1 mol/L醋酸溶液中加入少量NaOH溶液,溶液中c(CH3COO-)减少 |
| C、向0.1 mol/L醋酸溶液中不断加水,溶液中c(H+)增大 |
| D、向0.1 mol/L醋酸溶液中滴入少量浓盐酸,溶液的导电性减弱 |
下列各有机物的分类或命名正确的是( )
A、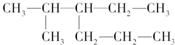 2甲基3丙基戊烷 2甲基3丙基戊烷 |
B、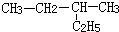 2-乙基丁烷 2-乙基丁烷 |
C、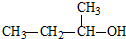 2-甲基-1-丙醇 2-甲基-1-丙醇 |
D、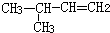 3-甲基-1-丁烯 3-甲基-1-丁烯 |
下列离子方程式书写正确的是( )
| A、NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | ||||
| B、将标准状况下112 mL氯气通入10 mL 1 mol?L-1的溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 | ||||
C、用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O
| ||||
| D、向澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
下列实验操作会引起测定结果偏高的是( )
| A、用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,读取滴定管末读数时,仰视刻度线 |
| B、测定硫酸铜晶体中结晶水含量的实验时,加热时间过短未完全变白 |
| C、中和滴定时,加待测液前锥形瓶内有少量水 |
| D、测定1mol氢气体积的操作中,反应结束后未抽气 |