题目内容
下表是元素周期表的一部分,针对表中的①~⑧中元素,用元素符号或化学式填空回答以下问题:
(1)在这些元素中,金属性最强的元素是 ,最活泼的非金属元素是 ;
(2)化学性质最不活泼的元素是 ,其原子的原子结构示意图为 ;
(3)元素的最高价氧化物对应的水化物中酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 ;
(4)在③~⑦元素中,原子半径最大的是 ,原子半径最小的是 ;
(5)在⑥与⑦的单质中,化学性质较活泼的是 ,设计一个实验方案比较其氧化性的强弱(用反应的化学方程式表示): .
 |
ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)化学性质最不活泼的元素是
(3)元素的最高价氧化物对应的水化物中酸性最强的是
(4)在③~⑦元素中,原子半径最大的是
(5)在⑥与⑦的单质中,化学性质较活泼的是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中的位置可知,①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为S、⑦为Cl、⑧为Ar,
(1)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱;
(2)稀有气体最外层为稳定结构,化学性质最不活泼;
(3)F元素没有最高价含氧酸,元素的最高价氧化物对应的水化物中酸性最强的是高氯酸;Na的金属性最强,元素的最高价氧化物对应的水化物的碱性最强,氢氧化铝是两性氢氧化物;
(4)同周期自左而右原子半径减小;
(5)同周期自左而非金属性增强,单质的活泼性最强,元素单质之间的置换反应等可以说明单质的氧化性强弱.
(1)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱;
(2)稀有气体最外层为稳定结构,化学性质最不活泼;
(3)F元素没有最高价含氧酸,元素的最高价氧化物对应的水化物中酸性最强的是高氯酸;Na的金属性最强,元素的最高价氧化物对应的水化物的碱性最强,氢氧化铝是两性氢氧化物;
(4)同周期自左而右原子半径减小;
(5)同周期自左而非金属性增强,单质的活泼性最强,元素单质之间的置换反应等可以说明单质的氧化性强弱.
解答:
解:由元素在周期表中的位置可知,①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为S、⑦为Cl、⑧为Ar,
(1)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,在这些元素中,金属性最强的元素是Na,最活泼的非金属元素是F,
故答案为:Na;F;
(2)稀有气体Ar最外层为稳定结构,化学性质最不活泼,其原子结构示意图为: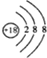 ,故答案为:Ar;
,故答案为:Ar; ;
;
(3)F元素没有最高价含氧酸,元素的最高价氧化物对应的水化物中酸性最强的是HClO4;Na的金属性最强,NaOH的碱性最强,Al(OH)3是两性氢氧化物,
故答案为:HClO4;NaOH;Al(OH)3;
(4)同周期自左而右原子半径减小,故在③~⑦元素中,原子半径最大的是Na,原子半径最小的是Cl,故答案为:Na;Cl;
(5)同周期自左而非金属性增强,单质的活泼性最强,故Cl2较硫活泼,Cl2+H2S=S↓+2HCl等可以说明单质的氧化性强弱,
故答案为:Cl2;Cl2+H2S=S↓+2HCl.
(1)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,在这些元素中,金属性最强的元素是Na,最活泼的非金属元素是F,
故答案为:Na;F;
(2)稀有气体Ar最外层为稳定结构,化学性质最不活泼,其原子结构示意图为:
 ,故答案为:Ar;
,故答案为:Ar; ;
;(3)F元素没有最高价含氧酸,元素的最高价氧化物对应的水化物中酸性最强的是HClO4;Na的金属性最强,NaOH的碱性最强,Al(OH)3是两性氢氧化物,
故答案为:HClO4;NaOH;Al(OH)3;
(4)同周期自左而右原子半径减小,故在③~⑦元素中,原子半径最大的是Na,原子半径最小的是Cl,故答案为:Na;Cl;
(5)同周期自左而非金属性增强,单质的活泼性最强,故Cl2较硫活泼,Cl2+H2S=S↓+2HCl等可以说明单质的氧化性强弱,
故答案为:Cl2;Cl2+H2S=S↓+2HCl.
点评:本题考查元素周期表与元素周期律,侧重对元素周期律的考查,难度不大,注意对基础知识的理解掌握.

练习册系列答案
相关题目
下列哪种方法不能增大铁跟盐酸反应的速率( )
| A、用粉末状铁代替块状铁 |
| B、用1mol?L-1HCl代替0.1mol?L-1HCl |
| C、增大压强 |
| D、改用不纯的铁代替纯铁 |
下列变化必须加入氧化剂才能实现的是( )
| A、NaHCO3→CO2 |
| B、Cl2→HClO |
| C、FeO→Fe3O4 |
| D、KMnO4→MnCl2 |
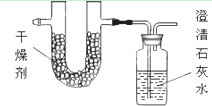 某烃CxHy同温同压条件下测得其蒸汽的密度是H2的43倍;将a g该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).
某烃CxHy同温同压条件下测得其蒸汽的密度是H2的43倍;将a g该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).