题目内容
3-对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
 +CO
+CO
A
B

E
已知:HCHO+CH3CHO
CH2=CHCHO+H2O.
(1)遇FeCl3溶液显紫色的A的同分异构体有 种.B中含氧官能团的名称为 .
(2)1molB最多能跟 molH2发生加成反应.
(3)试剂C可选用下列中的 .
a、溴水 b、银氨溶液 c、酸性KMnO4溶液 d、新制Cu(OH)2悬浊液
(4) 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为 .
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为 .
(5)E在一定条件下可以生成高聚物F,F的结构简式为 .
 +CO
+CO| AlCl3、HCl |
| 加热 |

| CH3CHO |
| OH-、加热 |
| ①C |
| ②H+ |

| CH3OH |
| H2SO4,加热 |
已知:HCHO+CH3CHO
| OH-、加热 |
(1)遇FeCl3溶液显紫色的A的同分异构体有
(2)1molB最多能跟
(3)试剂C可选用下列中的
a、溴水 b、银氨溶液 c、酸性KMnO4溶液 d、新制Cu(OH)2悬浊液
(4)
 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为(5)E在一定条件下可以生成高聚物F,F的结构简式为
考点:有机物的合成
专题:
分析:由合成路线可知,甲苯发生取代反应生成A对甲基苯甲醛,再与CH3CHO在碱性条件下反应生成B,B为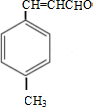 ,反应①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到
,反应①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到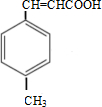 ,
, 与甲醇发生酯化反应生成E为
与甲醇发生酯化反应生成E为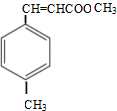 ,然后结合有机物的结构与性质来解答.
,然后结合有机物的结构与性质来解答.
 ,反应①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到
,反应①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到 ,
, 与甲醇发生酯化反应生成E为
与甲醇发生酯化反应生成E为 ,然后结合有机物的结构与性质来解答.
,然后结合有机物的结构与性质来解答.解答:
解:由合成路线可知,甲苯发生取代反应生成对甲基苯甲醛,再与CH3CHO在碱性条件下反应生成B,B为 ,①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到
,①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到 ,
, 与甲醇发生酯化反应生成E为
与甲醇发生酯化反应生成E为 ,
,
(1)遇FeCl3溶液显紫色,则含酚-OH,且苯环上有两个取代基,另一取代基为-CH=CH2,则符合条件的A的同分异构体为邻、间、对乙烯基苯酚3种,B中含氧官能团的名称为醛基,
故答案为:3;醛基;
(2)B为 ,其中含有一个苯环、一个碳碳双键、一个醛基,所以1molB最多能跟5molH2发生加成反应,
,其中含有一个苯环、一个碳碳双键、一个醛基,所以1molB最多能跟5molH2发生加成反应,
故答案为:5;
(3)试剂C不能与C=C反应,只氧化-CHO,则C为b或d,
故答案为:b、d;
(4)E的同分异构体中含-COOC-会发生水解,与足量NaOH溶液共热的化学方程式为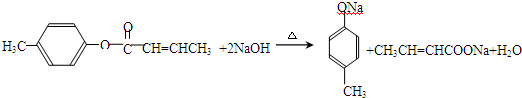 ,
,
故答案为: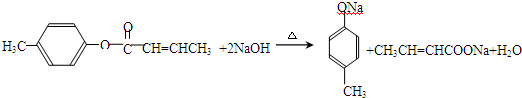 ;
;
(5)E中含C=C,在一定条件下可以生成高聚物F,发生加聚反应,则F的结构简式为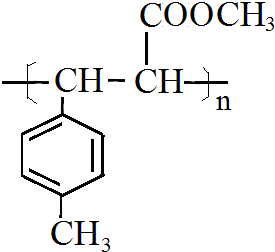 ,
,
故答案为: .
.
 ,①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到
,①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到 ,
, 与甲醇发生酯化反应生成E为
与甲醇发生酯化反应生成E为 ,
,(1)遇FeCl3溶液显紫色,则含酚-OH,且苯环上有两个取代基,另一取代基为-CH=CH2,则符合条件的A的同分异构体为邻、间、对乙烯基苯酚3种,B中含氧官能团的名称为醛基,
故答案为:3;醛基;
(2)B为
 ,其中含有一个苯环、一个碳碳双键、一个醛基,所以1molB最多能跟5molH2发生加成反应,
,其中含有一个苯环、一个碳碳双键、一个醛基,所以1molB最多能跟5molH2发生加成反应,故答案为:5;
(3)试剂C不能与C=C反应,只氧化-CHO,则C为b或d,
故答案为:b、d;
(4)E的同分异构体中含-COOC-会发生水解,与足量NaOH溶液共热的化学方程式为
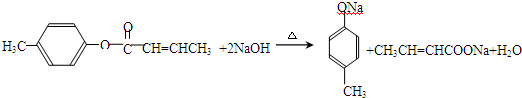 ,
,故答案为:
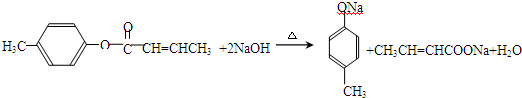 ;
; (5)E中含C=C,在一定条件下可以生成高聚物F,发生加聚反应,则F的结构简式为
 ,
,故答案为:
 .
.
点评:本题主要考查有机物的合成、结构与性质,把握合成流程中的反应及官能团、结构变化推断物质为解答的关键,注意酚、酯的性质,(4)为解答的易错点,题目难度中等.

练习册系列答案
相关题目
科学家发现一种新型氧分子,化学式为O4,在相同条件下,等质量的O2和O4具有相同的( )
| A、原子数 | B、分子数 |
| C、体积 | D、物质的量 |
金属-硫电池价格低廉,使用寿命较长,能量密度高,因而在电池研究领域得到广泛关注.最近,我国科研工作者研究了一种能在室温下工作的新型Na-S电池.该电池放电过程的总反应方程式如下:nS+2Na=Na2Sn (注:能量密度指单位质量的电极材料可输出的电能,以W?h?kg-1为计量单位),则下列说法不正确的是( )
| A、该电池中用固态金属Na为负极,S单质作为正极,但S单质须负载在导电材料上 |
| B、该电池的电解质必须具备室温下传导Na+的能力,但不宜用NaOH溶液作为电解液 |
| C、n值越大则该电池的能量密度越高 |
| D、该电池充电过程中阳极的电极反应式:Na2Sn-2e-=2Na++nS,故充电时Na+从阳极向阴极迁移 |
Al2O3MgO混合物溶于250mL盐酸得到无色溶液,逐滴加入0.5moL/LNaoH溶液,如图下列说法错误的是( )


| A、盐酸的物质的量浓度为0.22mol/L |
| B、混合物中Al2O3的物质的量为0.01mol |
| C、混合物中MgO的物质的量为0.01mol |
| D、P点加入NaOH溶液的体积是110mL |
 温度为T时,向2.00L恒容密闭容器中充入1.00molCH4,发生反应:2CH4(g)
温度为T时,向2.00L恒容密闭容器中充入1.00molCH4,发生反应:2CH4(g)
| ||
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(CH4)/mol | 1.00 | 0.84 | 0.81 | 0.80 | 0.80 |
| A、温度T时,前5s H2平均速率为0.024mol?L-1?s-1 |
| B、温度T时,b点 υ(逆)>υ(正) |
| C、该反应的平衡常数随温度升高逐渐减小 |
| D、温度T时,若向2.00L恒容密闭充入2.00molC2H2和6.00molH2,达到平衡时,C2H2转化率大于80% |
某无色溶液中,常温下由水电离出的c(H+)=1×10-14 mol/L,则该溶液中一定能大量共存的离子是( )
| A、Al3+、Na+、MnO4-、SO42- |
| B、Na+、Ag+、Cl-、NO3-、 |
| C、Na+、K+、Cl-、NO3- |
| D、K+、Ba2+、Cl-、HCO3- |
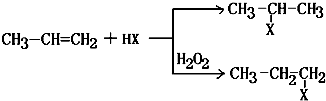 (X)为卤素原子
(X)为卤素原子 的物质,该物质是一种香料.
的物质,该物质是一种香料.
