题目内容
甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
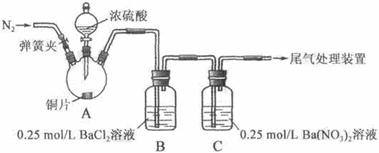
实验操作和现象:
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 |
|
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
⑴A中反应的化学方程式是 。
⑵C中白色沉淀是 ,该沉淀的生成表明SO2具有 性。
⑶C中液面上方生成浅棕色气体的化学方程式是 。
⑷分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是 ;
乙在A、B间增加洗气瓶D,D中盛放的试剂是 。
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
②进行实验,B中现象:
检验白色沉淀,发现均不溶于稀盐酸。结合离子方程式解释实验现象异同的原因: 。
⑸合并⑷中两同学的方案进行实验。B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是 。
.⑴Cu+2H2SO4![]() CuSO4+SO2↑+2H2O ⑵H2SO4 还原 ⑶2NO+O2
CuSO4+SO2↑+2H2O ⑵H2SO4 还原 ⑶2NO+O2![]() 2NO2 ⑷①通N2一段时间,排除装置中的空气 饱和NaHSO3溶液 ②甲:SO42-+Ba2+
2NO2 ⑷①通N2一段时间,排除装置中的空气 饱和NaHSO3溶液 ②甲:SO42-+Ba2+![]() BaSO4↓,乙:2Ba2++2SO2+O2+2H2O
BaSO4↓,乙:2Ba2++2SO2+O2+2H2O![]() 2BaSO4↓+4H+ 白雾的量远多于装置中O2的量 ⑸SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀
2BaSO4↓+4H+ 白雾的量远多于装置中O2的量 ⑸SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀
解析:本题主要考查了SO2的制取、性质及BaSO3、BaSO4的性质知识等,同时考查了学生的实验设计、分析、检验、推断等基本技能,充分考查了学生的思维分析能力等。
由题给实验目的和实验可知,A中发生的反应方程式为:Cu+2H2SO4![]() CuSO4+SO2↑+2H2O;A中白雾可能含有SO3或H2SO4,因B中白色沉淀不溶于稀盐酸,说明该白色沉淀为BaSO4,不是BaSO3;同理,C中的白色沉淀也是BaSO4,并因此说明SO2具有还原性;C中液面上方生成浅棕色气体则是硝酸还原生成的NO遇O2生成了红棕色的NO2之故,化学方程式是2NO+O2
CuSO4+SO2↑+2H2O;A中白雾可能含有SO3或H2SO4,因B中白色沉淀不溶于稀盐酸,说明该白色沉淀为BaSO4,不是BaSO3;同理,C中的白色沉淀也是BaSO4,并因此说明SO2具有还原性;C中液面上方生成浅棕色气体则是硝酸还原生成的NO遇O2生成了红棕色的NO2之故,化学方程式是2NO+O2![]() 2NO2;甲同学为排除装置内空气对实验结果的影响,在Cu与浓硫酸反应前,可先通一会儿N2;乙同学为除去白雾或SO2中的SO3,可在A、B间增加一个盛放浓硫酸或饱和NaHSO3溶液的洗气瓶;在甲、乙两同学的实验中,B中均出现了不溶于稀盐酸的白色沉淀,说明该白色沉淀都是BaSO4,由于甲同学没有排除白雾的干扰,故生成BaSO4沉淀的离子方程式为SO42-+Ba2+
2NO2;甲同学为排除装置内空气对实验结果的影响,在Cu与浓硫酸反应前,可先通一会儿N2;乙同学为除去白雾或SO2中的SO3,可在A、B间增加一个盛放浓硫酸或饱和NaHSO3溶液的洗气瓶;在甲、乙两同学的实验中,B中均出现了不溶于稀盐酸的白色沉淀,说明该白色沉淀都是BaSO4,由于甲同学没有排除白雾的干扰,故生成BaSO4沉淀的离子方程式为SO42-+Ba2+![]() BaSO4↓;乙同学没有排除空气的干扰,其生成BaSO4的离子方程式为2Ba2++2SO2+O2+2H2O
BaSO4↓;乙同学没有排除空气的干扰,其生成BaSO4的离子方程式为2Ba2++2SO2+O2+2H2O![]() 2BaSO4↓+4H+;合并甲、乙两同学的方案进行实验时,B中无沉淀生成,C中产生白色沉淀,说明SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀。
2BaSO4↓+4H+;合并甲、乙两同学的方案进行实验时,B中无沉淀生成,C中产生白色沉淀,说明SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀。

 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案黄铁矿石的主要成分为FeS2和少量FeS(假设其他杂质中不含Fe、S元素,且高温下不发生化学变化),是我国大多数硫酸厂制取硫酸的主要原料.某化学兴趣小组对该黄铁矿石进行如下实验探究.
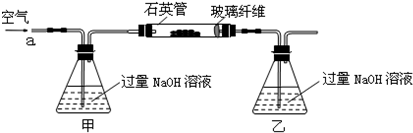
将m1g该黄铁矿石的样品放入如下图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全.其反应的化学方程式为:
4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
4FeS+7O2 2Fe2O3+4SO2
2Fe2O3+4SO2
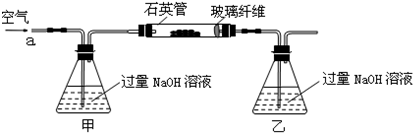
实验一:测定硫元素的含量
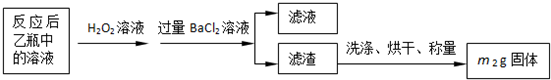
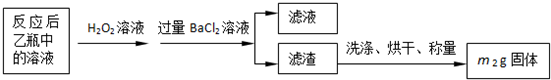
反应结束后,将乙瓶中的溶液进行如下处理:
(1)甲、乙两装置的作用分别是______、______;
乙瓶内发生反应的离子方程式为______、______;
(2)反应后乙瓶中的溶液需加足量H2O2溶液的目的是______.
(3)该黄铁矿石中硫元素的质量分数为______.
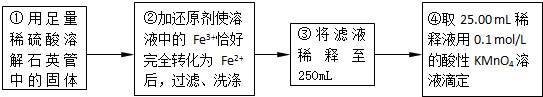
实验二:测定铁元素的含量
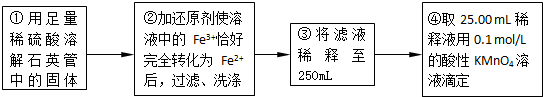
(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量______(填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有______.
(6)某同学一共进行了三次滴定实验,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液体积/mL | 25.00 | 25.03 | 24.97 |
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol?L-1 | c(H2SO4)/mol?L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.1 | 0.2 |
| ③ | 50 | 0.2 | 0.1 |
| ④ | 50 | 0.1 | 0.1 |
探究温度对化学反应速率的影响,应选择______(填实验编号).
(2)已知Na2S2O3溶液与Cl2反应时,1mol Na2S2O3转移8mol电子.该反应的离子方程式是______.
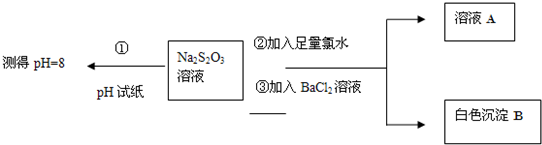
甲同学设计如下实验流程探究Na2S2O3的化学性质.
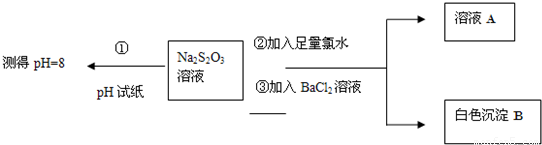
(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和______性.
(Ⅱ)生成白色沉淀B的离子方程式是______.
(Ⅲ)乙同学认为应将上述流程中②③所加试剂顺序颠倒,你认为甲、乙两同学的设计更合理的是______(填“甲”或“乙”),理由是______.