题目内容
PH=3和PH=5的盐酸等体积混合后溶液的PH是( )
| A、3.3 | B、3 | C、5 | D、4.7 |
考点:pH的简单计算
专题:
分析:酸溶液混合,先计算混合后溶液中氢离子的物质的量,再根据c=
计算氢离子的物质的量浓度,最后根据pH=-lgc(H+)计算出混合液的pH.
| n |
| V |
解答:
解:pH=3的盐酸和pH=5的硫酸等体积混合后,设体积均为VL,
混合液中氢离子的物质的量为:n(H+)=VL×10-3mol/L+VL×10-5mol/L≈10-3Vmol,
则混合溶液中氢离子浓度为:c(H+)=
=5×10-4mol/L,
所以pH=-lg5×10-4=4-lg5=3.3,
故选A.
混合液中氢离子的物质的量为:n(H+)=VL×10-3mol/L+VL×10-5mol/L≈10-3Vmol,
则混合溶液中氢离子浓度为:c(H+)=
| 10-3mol |
| 2VL |
所以pH=-lg5×10-4=4-lg5=3.3,
故选A.
点评:本题考查了混合液的pH的计算,题目难度不大,试题侧重基础知识的考查,注意掌握pH的表达式及计算方法,明确溶液酸碱性与溶液pH的关系为解答关键,试题有利于培养学生的化学计算能力.

练习册系列答案
相关题目
测定稀盐酸和氢氧化钠稀溶液中和热的实 验中没有使用的仪器有:①大、小烧杯;②容量瓶;③量筒;④环形玻璃搅拌棒;⑤试管;⑥温度计;⑦蒸发皿;⑧托盘天平中的( )
| A、②⑤⑦⑧ | B、①②⑥⑦ |
| C、②③⑦⑧ | D、③④⑤⑦ |
要鉴别己烯中是否混有少量甲苯,正确的实验方法是( )
| A、点燃这种液体,然后观察火焰的颜色 |
| B、先加足量酸性高锰酸钾溶液,然后再加入溴水 |
| C、加入浓硫酸与浓硝酸后加热 |
| D、先加足量溴水,然后再加入酸性高锰酸钾溶液 |
下列有关金属钠的说法中,错误的是( )
| A、钠只有在加热条件下才能与氯气反应 |
| B、钠与氧气反应的产物与反应条件有关 |
| C、工业上通过电解熔融NaCl制备金属钠 |
| D、实验室常将钠保存在煤油中 |
难挥发性二硫化钽(TaS2)可采用如图装置提纯.将不纯的TaS2粉末装入石英管一端,抽真空后加入适量碘并封管,置于加热炉中,发生反应:TaS2(s)+2I2(g)
TaI4(g)+S2(g).下列说法正确的是( )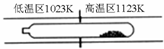
| 1123K |
| 1023K |

| A、在不同温度区域,TaI4的量保持不变 |
| B、在提纯过程中,I2的量不断减少 |
| C、该反应的平衡常数与TaI4和S2的浓度乘积成反比 |
| D、在提纯过程中,I2的作用是将TaS2从高温区转移到低温区 |
如果Mg2-、NO3-、Na-和M四种离子以物质的量之比为1:2:4:2共同存在同一种溶液中,那么M可能是( )
| A、K+ |
| B、Cl- |
| C、CO32- |
| D、SO42- |
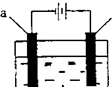 下列对如图所示装置实验现象的描述正确的是( )
下列对如图所示装置实验现象的描述正确的是( )