题目内容
 准确称取6克铝土矿样品(含Al2O3、Fe2O3、SiO2)加入100mL硫酸溶液,充分反应后,
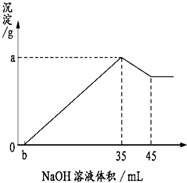
准确称取6克铝土矿样品(含Al2O3、Fe2O3、SiO2)加入100mL硫酸溶液,充分反应后,向滤液中加入10mol/L NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,求所用硫酸溶液的物质的量浓度( )
| A、1.75 mol/L |
| B、3.5 mol/L |
| C、2.25 mol/L |
| D、无法计算 |
考点:有关混合物反应的计算,镁、铝的重要化合物
专题:图示题
分析:加入35mL氢氧化钠溶液时,沉淀量最大,此时溶液中溶质为Na2SO4,根据钠离子守恒计算硫酸钠的物质的量,再根据硫酸根守恒计算原硫酸溶液中n(H2SO4),再根据c=
计算.
| n |
| V |
解答:
解:当加入NaOH溶液的体积为35mL时,n(NaOH)=0.035L×10mol/L=0.35mol,此时沉淀的质量达到最大值,则此时溶液的溶质只有Na2SO4,
根据Na元素守恒有n(Na2SO4)=
n(NaOH)=
×0.35mol=0.175mol,
根据硫酸根守恒,则有:n(H2SO4)=0.175mol,
所以原硫酸溶液中c(H2SO4)=
=1.75mol/L,
故选A.
根据Na元素守恒有n(Na2SO4)=
| 1 |
| 2 |
| 1 |
| 2 |
根据硫酸根守恒,则有:n(H2SO4)=0.175mol,
所以原硫酸溶液中c(H2SO4)=
| 0.175mol |
| 0.1L |
故选A.
点评:本题考查混合物的有关计算,难度中等,清楚图象中各阶段发生的反应是关键,注意根据守恒的计算,关键是判断沉淀最大值时溶液中的溶质.

练习册系列答案
相关题目
体积相同的甲乙两容器中,分别充入1molA和1molB,在相同温度下发生反应:2A(g)+B(g)?2C(g) 并达到平衡,甲容器保持体积不变,C的体积分数为m%;乙容器保持压强不变,C的体积分数为n%,则m和n的正确关系为( )
| A、m<n | B、m=n |
| C、m>n | D、无法比较 |
镁、铝、铁合金投入到300ml硝酸溶液中,金属恰好溶解,转化成Mg2+、Al3+和Fe3+;硝酸全部被还原为NO,且在标准状况下,体积为6.72L,当加入300ml某浓度NaOH,金属阳离子恰好全部沉淀,干燥后测得质量为27.2g.下列有关推断正确的是( )
| A、参加反应HNO3物质的量为0.9mol |
| B、参加反应的金属质量为11.9g |
| C、HNO3物质的量浓度为3mol/L |
| D、NaOH物质的量浓度为6mol/L |
当下列各组物质的总物质的量保持不变时,组内各成分以任意比例混合充分燃烧,消耗O2的量和生成的CO2的量都不变的是( )
| A、乙烯 乙醛 |
| B、乙炔 乙二醇 |
| C、甲烷 甲醇 |
| D、甲烷 乙醇 |
下列有关环境污染的说法正确的是( )
| A、燃煤时加入适量石灰石,可减少废气SO2的排放量 |
| B、空气中臭氧的含量越高,对人体健康越有利 |
| C、PH在5.6-7之间的降水通常称为酸雨 |
| D、含磷洗涤剂易于被细菌分解,故不会导致水体污染 |
在常温下,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、.0.1mol?L-1 pH=7.82的NH4HCO3溶液中:c(HCO3-)>c(NH4+)>c(OH-)>c(H+) |
| B、浓度均为0.1mol?L-1的NH3?H2O溶液和NH4Cl溶液等体积混合:[c(NH4+)+c(H+)]>[c(NH3?H2O)+c(OH-)] |
| C、0.1mol?L-1Na2S溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| D、0.1mol?L-1Na2S溶液与0.1mol?L-1 NaHS溶液等体积混合:2c(Na+)-3c(S2-)=3c(HS-)+3c(H2S) |
下列实验结论或操作、生产方法,准确合理的是( )
| A、某钠盐溶于盐酸产生能使澄清石灰水变浑浊的无色无味气体,说明该钠盐是Na2CO3 |
| B、用饱和Na2CO3溶液除去CO2中混有的HCl |
| C、工业上常采用电解熔融MgO的方法制取金属镁 |
| D、除去MgCl2溶液中少量FeCl3可向其中加入足量Mg(OH)2粉末,充分搅拌后过滤 |