题目内容
下列表示物质结构的化学用语或模型中,正确的是( )
A、HF的电子式: | ||
B、Cl-离子的结构示意图: | ||
C、8个中子的碳原子的核素符号
| ||
D、CH4分子的 球棍模型: 球棍模型: |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氟化氢为共价化合物,分子中不存在阴阳离子;
B.氯离子与氯原子的核电荷数相等,氯离子的核电荷数为17,不是18;
C.碳原子的质子数为6,中子数为8的碳原子的质量数为14;
D.根据甲烷的球棍模型与比例模型的表示方法进行判断.
B.氯离子与氯原子的核电荷数相等,氯离子的核电荷数为17,不是18;
C.碳原子的质子数为6,中子数为8的碳原子的质量数为14;
D.根据甲烷的球棍模型与比例模型的表示方法进行判断.
解答:
解:A.氟化氢属于共价化合物,其分子中存在1个F-H共用电子对,氟化氢正确的电子式为: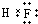 ,故A错误;
,故A错误;
B.氯离子的核电荷数为17,核外电子总数为18,最外层为8个分子,氯离子正确的结构示意图为: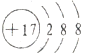 ,故B错误;
,故B错误;
C.8个中子的碳原子的质量数为14,碳原子的质子数为6,该核素符号可以表示为
C,故C正确;
D. 主要体现原子的相对体积大小,为甲烷的比例模型,甲烷的球棍模型为:
主要体现原子的相对体积大小,为甲烷的比例模型,甲烷的球棍模型为: ,故D错误;
,故D错误;
故选C.
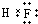 ,故A错误;
,故A错误;B.氯离子的核电荷数为17,核外电子总数为18,最外层为8个分子,氯离子正确的结构示意图为:
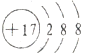 ,故B错误;
,故B错误;C.8个中子的碳原子的质量数为14,碳原子的质子数为6,该核素符号可以表示为
| : | 14 6 |
D.
 主要体现原子的相对体积大小,为甲烷的比例模型,甲烷的球棍模型为:
主要体现原子的相对体积大小,为甲烷的比例模型,甲烷的球棍模型为: ,故D错误;
,故D错误;故选C.
点评:本题考查了电子式、离子结构示意图、球棍模型与比例模型、元素符号等化学用语的判断,题目难度中等,注意掌握常见化学用语的概念及正确的表示方法,明确球棍模型与比例模型的区别.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列实验基本操作中,正确的是( )
A、 倾倒液体 |
B、 过滤 |
C、 加热液体 |
D、 熄灭酒精灯 |
下列有关实验的做法不正确的是( )
| A、分液操作时分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、容量瓶使用前需要检查是否漏水 |
| C、配置0.1000mol?L-1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流 |
| D、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
1gN2含有2m个原子,则阿伏加德罗常数的值可表示为( )
A、
| ||
| B、m | ||
| C、28m | ||
D、
|
下列对应的离子方程式正确的是( )
| A、Fe2(SO4)3的酸性溶液中通入足量硫化氢:Fe3++H2S═Fe2++S↓+2H+ |
| B、碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
| C、氯化铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ |
| D、澄清石灰水中通入过量CO2:OH-+CO2═HCO3- |
在一定条件下,按下列物质的量关系进行反应,其对应的离子方程式或化学方程式书写正确的是( )
点燃.
点燃.
A、n(Cl2):n(Fe)=5:4 5Cl2+4Fe
| ||||
| B、n(Cl2):n(FeBr2)=1:1 Fe2++2Br-+Cl2═Fe3++Br2+2Cl- | ||||
| C、n(MnO4-):n(H2O2)=2:3 2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | ||||
| D、n(Fe):n(HNO3(稀))═1:3 4Fe+12H++3NO3-=3Fe2++Fe3++3NO↑+6H2O |
 中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示.
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示. 分子中n1=6、n2=1、n3=2、n4=1.试根据不同烷烃的组成结构,分析出烷烃(除甲烷外)各原子数的关系.
分子中n1=6、n2=1、n3=2、n4=1.试根据不同烷烃的组成结构,分析出烷烃(除甲烷外)各原子数的关系.