题目内容
(15分)1mol水蒸汽和炽热的焦炭反应生成水煤气,反应吸热131.4 kJ ·mol-1。利用该反应生成的氢气和空气中的氮气合成氨,其反应的△H<0。氨可以用于制备硝酸。请回答:
(1)生成水煤气的热化学方程式是 ;
(2)合成氨需要在较大的压力下进行的原因是 ;
(3)温度过高或过低对合成氨的影响是 ;
(4)由氨生成HNO3的各步反应的化学方程式是 ;
(5)某化肥厂由NH3制备HNO3,进而生产硝铵(NH4NO3)。假设由氨氧化生成HNO3的总产率是85%,而HNO3和NH3完全反应生成NH4NO3。列式计算:
①从NH3制取NH4NO3过程中,用于中和硝酸所需的氨占总的氨消耗量的分数;
②若氨的消耗总量为100 kg,可生产NH4NO3的量。
(1)C(s)+H2O(g)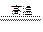 CO(g)+H2(g),△H =" +131.4" kJ ·mol-1
CO(g)+H2(g),△H =" +131.4" kJ ·mol-1
(2)合成氨是体积减少的反应,加大压力有利于平衡向生成氨的方向移动
(3)温度过低反应速率慢;合成氨为放热反应,温度过高反应向氨分解的方向进行
(4)4NH3+5NO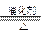 4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO
4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO
(5)①中和硝酸所需的氨占总的氨消耗量的分数为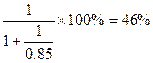
②可生产NH4NO3:100kg×46%×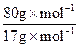 =216kg
=216kg
解析

练习册系列答案
相关题目