题目内容
15.按要求填空:(1)0.5molSO2共约含有9.03×1023个原子,它与40gSO3所含硫原子数相等.
(2)有100mL0.2mol/L的NaOH溶液,将此溶液稀释到200mL,则稀释后溶液中Na+的物质的量浓度是0.1mol/L.
(3)相同条件下,相同体积的 ①HCl、②NH3、③CO2、④O2四种气体中,含有电子数目由小到大的是(填序号)③①④②.
分析 (1)结合N=nNA、m=nM及物质的构成计算;
(2)稀释前后溶液中离子的物质的量不变,结合n=cV计算;
(3)相同条件下,相同体积,则物质的量相同,物质的量的量为1mol的①HCl、②NH3、③CO2、④O2四种气体含有电子数目分别为:18mol、10mol、22mol、16mol,由此解答.
解答 解:(1)0.5mol SO2共含0.5mol×3=1.5mol原子,约含有1.5×NA=9.03×1023个原子,由S原子守恒可知,与0.5molSO3所含硫原子数相等,其质量为0.5mol×80g/mol=40g,故答案为:9.03×1023;40;
(2)100mL 0.2mol/L的NaOH溶液,钠离子物质的量为0.1L×0.2mol/L=0.02mol,此溶液稀释到200mL,则稀释后溶液中Na+的物质的量浓度是0.1mol/L,故答案为:0.1mol/L;
(3)相同条件下,相同体积,则物质的量相同,物质的量的量为1mol的①HCl、②NH3、③CO2、④O2四种气体含有电子数目分别为:18mol、10mol、22mol、16mol,含有电子数目由小到大的是③①④②,故答案为:③①④②.
点评 本题考查物质的量的有关计算,为高频考点,把握质量、物质的量、体积及微粒数的关系为解答的关键,侧重分析能力及计算能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.维生素A对人体特别是对人的视力有重要作用,其结构简式如图所示:
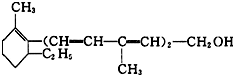
下述关于该化合物的说法正确的是( )

下述关于该化合物的说法正确的是( )
| A. | 维生素A的分子式为C16H25O | B. | 维生素A的一个分子中有3个双键 | ||
| C. | 维生素A含有苯环结构 | D. | 维生素A的分子中含有两种官能团 |
3.在下列物质中,在一定条件下能与某些酸、碱、金属、非金属都反应的是…( )(双选,请举例说明.)
| A. | Al2O3 | B. | H2SO3 | C. | H2S | D. | NaHCO3 |
10.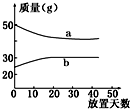 浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如右图所示,分析a、b曲线变化的原因是( )
浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如右图所示,分析a、b曲线变化的原因是( )
 浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如右图所示,分析a、b曲线变化的原因是( )
浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如右图所示,分析a、b曲线变化的原因是( )| A. | a升华、b冷凝 | B. | a蒸发、b吸水 | C. | a蒸发、b潮解 | D. | a冷凝、b吸水 |
4.下列有关物质应用的叙述中,不正确的是( )
| A. | 氢氧化铝可用于治疗胃酸过多 | |
| B. | ClO2用于饮用水消毒 | |
| C. | 水玻璃浸泡过的木材既能防腐又能耐火 | |
| D. | Si用于制造光导纤维 |
5.对分子量为104的烃的下列说法,正确的组合是( )
①可能是芳香烃 ②可能发生加聚反应 ③分子中不可能都是单键 ④分子中可能都是单键.
①可能是芳香烃 ②可能发生加聚反应 ③分子中不可能都是单键 ④分子中可能都是单键.
| A. | 只有①② | B. | 只有①③ | C. | 只有①②③ |
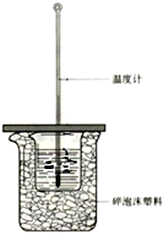 50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图上所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.
50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图上所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.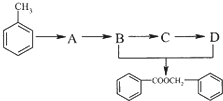
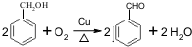 .
. 的化学方程式为
的化学方程式为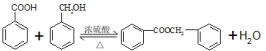 .
.