题目内容
16.下列反应中,在高温下不能自发进行的是( )| A. | MgCO3(s)═MgO(s)+CO2(g) | B. | 2N2O5(g)?4NO2(g)+O2(g) | ||
| C. | (NH4)2CO3(s)?NH3(g)+NH4HCO3(s) | D. | 2CO(g)?2C(s)+O2(g) |
分析 题中所给反应的焓变都大于零,反应如能在高温下自发进行,需满足△G=△H-T•△S<0,则熵变应大于零,否则不能自发进行.
解答 解:A.反应的△H>0,气体的物质的量增加△S>0,在高温下△G=△H-T•△S<0,反应能自发进行,故A不符合;
B、反应的△H>0,气体的物质的量增加△S>0,在高温下△G=△H-T•△S<0,反应能自发进行,故B不符合;
C、反应的△H>0,气体的物质的量增加△S>0,在高温下△G=△H-T•△S>0,反应高温下自发进行,故C不符合;
D、反应的△H>0,气体的物质的量减小△S<0,在高温下△G=△H-T•△S>0,反应不能自发进行,故D符合;
故选D.
点评 本题考查焓变和熵变,题目难度不大,注意选项中的反应都为分解反应,为吸热反应,结合△G=△H-T•△S<0时才能自发进行判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列烷烃在光照条件下与氯气反应,只生成一种一氯代烃的是( )
| A. | CH3CH2CH2CH3 | B. | CH3CH(CH3)CH3 | C. | C(CH3)4 | D. | CH3CH(CH3)CH2CH3 |
4.根据碳四价、氧二价、氢一价、氮三价的原则,可能成立的分子式是( )
| A. | C4H4 | B. | C7H15O | C. | C3H9O | D. | C4H7NO |
8.下列叙述正确是(用NA 代表阿伏加德罗常数的值)( )
| A. | 2.4g 金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 1mol甲烷分子所含质子数为10NA | |
| C. | 常温常压下,2g氢气含有的分子与32g氧气中分子数目均为NA | |
| D. | 4g氦气所含原子数为2NA |
11.用NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A. | 23gNa在氧气中完全燃烧失去NA个电子 | |
| B. | 常温常压下,6.2g Na2O含有的Na+离子数为0.2 NA | |
| C. | 标准状况下,22.4LH2O含有NA个分子 | |
| D. | 1L0.5 mol/LFe2(SO4)3溶液中,SO42-的数目为1.5NA |
 .
.
 .
.
 R可以被KMnO4的酸性溶液氧化生成
R可以被KMnO4的酸性溶液氧化生成 COOH,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到
COOH,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到 COOH.现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为
COOH.现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为 COOH的异构体共有7种,其中的3种是:
COOH的异构体共有7种,其中的3种是: CH2CH2CH2CH2CH3,
CH2CH2CH2CH2CH3,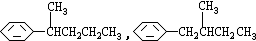
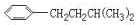 ,
,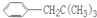 ,
,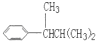 ,
, .
.