题目内容
按要求书写下列反应的离子方程式
(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性
(2)Ca(OH)2溶液与足量NaHCO3溶液反应
(3)足量Ca(OH)2溶液与NaHCO3溶液反应
(4)硝酸银和足量的氨水反应
(5)氯气和少量的溴化亚铁反应 .
(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性
(2)Ca(OH)2溶液与足量NaHCO3溶液反应
(3)足量Ca(OH)2溶液与NaHCO3溶液反应
(4)硝酸银和足量的氨水反应
(5)氯气和少量的溴化亚铁反应
考点:离子方程式的书写
专题:离子反应专题
分析:(1)当氢离子和氢氧根离子恰好完全反应时溶液为中性;
(2)Ca(OH)2溶液与足量NaHCO3反应,氢氧根离子被完全中和;
(3)足量Ca(OH)2溶液与NaHCO3溶液反应碳酸氢根离子完全转化为沉淀;
(4)硝酸银与足量的氨水反应生成银氨溶液;
(5)氯气足量,所以溴离子、二价铁离子都被氧化.
(2)Ca(OH)2溶液与足量NaHCO3反应,氢氧根离子被完全中和;
(3)足量Ca(OH)2溶液与NaHCO3溶液反应碳酸氢根离子完全转化为沉淀;
(4)硝酸银与足量的氨水反应生成银氨溶液;
(5)氯气足量,所以溴离子、二价铁离子都被氧化.
解答:
解:(1)向NaHSO4溶液中滴入Ba(OH)2溶液,当氢氧根离子恰好被完全中和时溶液为中性,所以离子方程式为Ba2++SO42-+2OH-+2H+=BaSO4↓+2H2O,
故答案为:Ba2++SO42-+2OH-+2H+=BaSO4↓+2H2O;
(2)NaHCO3溶液与Ca(OH)2溶液反应,NaHCO3足量,氢氧化钙中氢氧根离子完全被中和,则反应的离子方程式为:2HCO3-+2OH-+Ca2+=CaCO3↓+2H2O+CO32-,
故答案为:2HCO3-+2OH-+Ca2+=CaCO3↓+2H2O+CO32-;
(3)足量Ca(OH)2溶液与NaHCO3溶液反应碳酸氢根离子完全转化为沉淀,则反应的离子方程式为:HCO3-+OH-+Ca2+=CaCO3↓+H2O,
故答案为:HCO3-+OH-+Ca2+=CaCO3↓+H2O;
(4)硝酸银与足量的氨水反应生成银氨溶液,其反应方程式为:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O,
故答案为:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O;
(5)足量的氯气通入到溴化亚铁溶液中的离子方程式为:3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2,故答案为:3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2.
故答案为:Ba2++SO42-+2OH-+2H+=BaSO4↓+2H2O;
(2)NaHCO3溶液与Ca(OH)2溶液反应,NaHCO3足量,氢氧化钙中氢氧根离子完全被中和,则反应的离子方程式为:2HCO3-+2OH-+Ca2+=CaCO3↓+2H2O+CO32-,
故答案为:2HCO3-+2OH-+Ca2+=CaCO3↓+2H2O+CO32-;
(3)足量Ca(OH)2溶液与NaHCO3溶液反应碳酸氢根离子完全转化为沉淀,则反应的离子方程式为:HCO3-+OH-+Ca2+=CaCO3↓+H2O,
故答案为:HCO3-+OH-+Ca2+=CaCO3↓+H2O;
(4)硝酸银与足量的氨水反应生成银氨溶液,其反应方程式为:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O,
故答案为:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O;
(5)足量的氯气通入到溴化亚铁溶液中的离子方程式为:3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2,故答案为:3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2.
点评:本题考查离子反应方程式书写,把握发生的反应及离子反应的书写方法为解答的关键,注意反应物之间物质的量关系,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
分类是化学学习和研究中的常用手段,下列分类依据和结论都正确的是( )
| A、浓盐酸、浓硫酸、浓硝酸均具有氧化性,都属氧化性酸 |
| B、Na2O、SO2、BaSO4在熔融状态或溶于水时均能导电,都属电解质 |
| C、NaOH、HNO3、NaNO3在水溶液中均能电离出离子,都属离子化合物 |
| D、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为一类物质,分类标准是可溶于水 |
下列叙述正确的是( )
| A、元素周期表中位于金属与非金属分界线附近的元素属于过渡元素 |
| B、短周期第IVA族与VIIA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
| C、C、N、O、H四种元素形成的化合物一定既有离子键又有共价键 |
| D、第三周期非金属元素含氧酸的酸性从左到右依次增强 |
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、1molNa2O2固体中含有的阴阳离子总数为4NA |
| B、标准状况下,11.2L四氯化碳中含有的C-CI键的个数为2NA |
| C、1L1 mol?L-1的NaClO溶液中含有ClO-的数目为NA |
| D、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
下列说法中正确的是( )
| A、摩尔是表示物质质量的单位 |
| B、10g氟化氢含有0.5molHF分子 |
| C、1g氢气的物质的量是1mol |
| D、物质的摩尔质量等于其式量 |
下列实验操作能达到实验目的是( )
| A、用加热蒸发Na2CO3溶液的方法除去少量NaHCO3 |
| B、向含有少量Fe3+的CuSO4溶液中加入铜片除去Fe3+ |
| C、用加热的方法分离NH4Cl和碘固体混合物 |
| D、用二氧化锰区别10%的H2O2溶液和10%的稀盐酸 |
下列物质中含有共价键的离子化合物是( )
①MgF2 ②Na2O2 ③NaOH ④CO2 ⑤NH4Cl ⑥H2O2 ⑦N2.
①MgF2 ②Na2O2 ③NaOH ④CO2 ⑤NH4Cl ⑥H2O2 ⑦N2.
| A、②③④⑤ | B、②③⑤ |
| C、①②③⑤ | D、①③⑤⑥ |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A、乙炔的结构简式:CHCH |
| B、乙酸乙酯的实验式C4H8O2 |
C、一氯甲烷的电子式: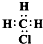 |
D、丙烷的球棍模型: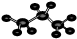 |