题目内容
一定量的锌与100 mL 18.0mol·L-1的浓H2SO4充分反应后,锌完全溶解,同时生成标准状况下的气体33.6 L。将反应后的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1。则下列说法中错误的是
A、生成的气体中SO2的物质的量为0.3mol
B、生成的气体中SO2的物质的量为0.25mol
C、溶解Zn的物质的量为1.5mol
D、反应中转移电子的物质的量为3mol
A
【解析】
试题分析:锌与浓硫酸发生:Zn+2H2SO4═ZnSO4+SO2↑+2H2O,随着反应的进行,硫酸浓度降低,发生:Zn+H2SO4═ZnSO4+H2↑,生成气体为SO2和H2的混合物,物质的量为33.6/22.4==1.5mol,剩余硫酸的物质的量为:n(H2SO4)=1/2×1L×0.1mol/L=0.05mol,
消耗硫酸的物质的量为:n(H2SO4)消耗=0.1L×18.0mol/L-0.05mol=1.75mol,
设混合物气体中含有xmolSO2,ymolH2,
Zn+2H2SO4═ZnSO4+SO2↑+2H2O Zn+H2SO4═ZnSO4+H2↑
2xmol xmol ymol ymol
则x+y=1.5 2x+y=1.75 解得x=0.25,y=1.25,
A.生成的气体中SO2的物质的量为0.25mol,A错误;B.生成的气体中SO2的物质的量为0.25mol,B正确;C、溶解Zn的物质的量为(0.25+1.25)=1.5mol,C错误;D、反应中转移电子的物质的量为1.5x2=3mol,选A。
考点:考查氧化还原反应的计算。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

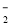 、CO
、CO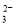
 广泛存在于食物中,它可能具有抗癌性,能与1mol该化合物 起反应的Br2或H2的最大用量分别为:
广泛存在于食物中,它可能具有抗癌性,能与1mol该化合物 起反应的Br2或H2的最大用量分别为: