��Ŀ����
1����ҵȼ��ú��ʯ�͵Ȼ�ʯȼ���ͷų������������NOx����CO2��SO2�����壬������Ⱦ�������Է���������������̼����������ʵ����ɫ�������������ã�����������֪��H2��ȼ����Ϊ285.8kJ•mol-1
N2��g��+2O2��g��=2NO2��g����H=+133kJ•mol-1
H2O��g��=H2O��l����H=-44kJ•mol-1
���������£�H2��ԭNO2����ˮ���������������ʵ��Ȼ�ѧ����ʽΪ4H2��g��+2NO2��g��=N2��g��+4H2O��g����H=-1100.2kJ•mol-1
����̼����2L�ܱ������м���2mol CO2��6mol H2�����ʵ��Ĵ��������£�������Ӧ��
CO2��g��+3H2��g��?CH3OH��l��+H2O��l��
��1���ٸ÷�Ӧ�Է����е������ǵ��£�����¡��������¡��������¶ȡ���
������������˵���˷�Ӧ�ﵽƽ��״̬����de��
a����������ƽ��ʽ�����ֲ��� b��CO2��H2������������ֲ���
c��CO2��H2��ת������� d�����������ܶȱ��ֲ���
e��1mol CO2���ɵ�ͬʱ��3mol H-H������
��2������״���������ȼ�ϵ�أ��õ���Dz��ò���̼������Ϊ�缫��������ϡ������Һ��ֱ�Ӽ��봿����ļ״���ͬʱ��һ���缫ͨ����������������ĵ缫��Ӧʽ��2CH3OH+2H2O-12e-�T12H++2CO2��
���� �������Ȼ�ѧ����ʽ��˹���ɼ��������Ȼ�ѧ����ʽ��
��1�����Է����е��ж������ǡ�H-T��S��0����Ϸ�Ӧ���������ж���Ҫ��������
��ƽ���־�����淴Ӧ������ͬ������ֺ������ֲ��䣬ԭ���DZ����������ѡ�
��2��ȼ��ȼ��ʱ��ԭ����и�����ȼ��ʧ���ӷ���������Ӧ��
��� �⣺�� ��֪��H2����ֵΪ142.9KJ•g-1 ��ȼ����Ϊ285.8KJ/mol��
��H2��g��+$\frac{1}{2}$O2��g��=H2O��l����H=-285.8KJ/mol
��N2��g��+2O2��g��=2NO2��g����H=+133kJ•mol-1
��H2O��g��=H2O��l����H=-44kJ•mol-1
�١�4-��-�ۡ�4�õ����������£�H2��ԭNO2����ˮ���������������ʵ��Ȼ�ѧ����ʽΪ4H2��g��+2NO2��g��=N2��g��+4H2O��g����H=-1100.2kJ•mol-1��
�ʴ�Ϊ��4H2��g��+2NO2��g��=N2��g��+4H2O��g����H=-1100.2kJ•mol-1��
��1����CO2��g��+3H2��g���TCH3OH��l��+H2O��l�����ر��S��0����Ӧ�ʱ��H��0�������������H-T��S��0
�ʴ�Ϊ�����£�
��CO2��g��+3H2��g���TCH3OH��l��+H2O��l����
a����������ƽ��ʽ��ʼ�ձ��ֲ��䣬����˵����Ӧ�ﵽƽ��״̬����a����
b����2L�ܱ������м���2mol CO2��6mol H2������1��3��Ӧ�����Թ�����CO2��H2���������ʼ�ձ��ֲ��䣬��b����
c����2L�ܱ������м���2mol CO2��6mol H2������1��3��Ӧ��CO2��H2��ת����ʼ����ȣ�����ȷ����Ӧ�Ƿ�ﵽƽ��״̬����c����
d����Ӧ�������壬��������Һ�壬���������ܶȱ��ֲ��䣬˵����Ӧ�ﵽƽ��״̬����d��ȷ��
e��1mol CO2���ɵ�ͬʱ��3mol H-H�����ѣ�˵�����淴Ӧ������ͬ����Ӧ�ﵽƽ��״̬����e��ȷ��
�ʴ�Ϊ��d e��
��2���״�ȼ�ϵ�ع���ʱ��ԭ����и�����ȼ�ϼ״�ʧ���ӷ���������Ӧ��2CH3OH+2H2O-12e-�T12H++2CO2���ʴ�Ϊ��2CH3OH+2H2O-12e-�T12H++2CO2��
���� ���⿼�����Ȼ�ѧ����ʽ��д��ƽ��Ӱ�����ط����жϣ�ƽ�����ķ���Ӧ�ã�ע����º��ݺͺ��ݾ��������ķ����жϣ����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�

| A�� | I2 | B�� | NaIO | C�� | KI | D�� | KIO3 |
| A�� | �������� | B�� | ����Ĥ | C�� | ��� | D�� | ���ʯ |
| A�� | 0.03mol•L-1��������Һ | B�� | 0.03mol•L-1��BaCl2��Һ | ||
| C�� | 0.04mol•L-1��NaCl��Һ | D�� | 0.02mol•L-1��CH3COOH��Һ |
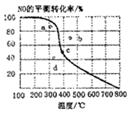 ��ͼ������Ϊһ��ѹǿ��NO��ƽ��ת�������¶ȵĹ�ϵ��ͼ��a��b��c��d�ĵ��ʾ��ͬ�¶ȡ�ѹǿ��2NO��g��+O2��g��?2NO2��g���ﵽƽ��ʱNO��ת���ʣ���ѹǿ���ĵ�Ϊ��������
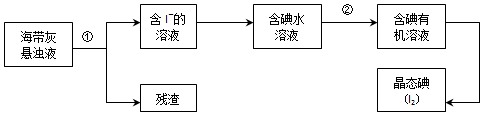
��ͼ������Ϊһ��ѹǿ��NO��ƽ��ת�������¶ȵĹ�ϵ��ͼ��a��b��c��d�ĵ��ʾ��ͬ�¶ȡ�ѹǿ��2NO��g��+O2��g��?2NO2��g���ﵽƽ��ʱNO��ת���ʣ���ѹǿ���ĵ�Ϊ��������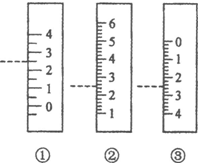 ��������У��ѧ��ȤС���ͬѧ�ⶨ����ʳ���д���Ũ�ȵ�ʵ�飬������벢������ʵ�飺
��������У��ѧ��ȤС���ͬѧ�ⶨ����ʳ���д���Ũ�ȵ�ʵ�飬������벢������ʵ�飺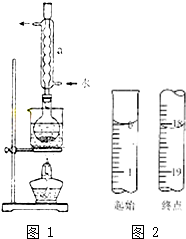 Na2S2O3����Ҫ�Ļ���ԭ�ϣ�������ˮ�������Ի���Ի������ȶ���
Na2S2O3����Ҫ�Ļ���ԭ�ϣ�������ˮ�������Ի���Ի������ȶ��� ���÷�Ӧ����ȡ�����ȡ�����ӳɡ�����Ӧ��
���÷�Ӧ����ȡ�����ȡ�����ӳɡ�����Ӧ��