题目内容
【化学一物质结构与性质】(15分)
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素n的基态原子的价电子排布式 ,元素O在周期表的位置是 ,属于 区。
(2)k在空气中燃烧产物的分子构型为 ,中心原子的杂化方式为 ,该分子是 (填“极性”或“非极性”)分子。
(3)第三周期8种元素按单质熔点高低的顺序如左下图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填下图中的序号)。

(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如右下图乙所示。则晶胞中i原子的配位数为 。

(1)3d54s1 (2分) 第四周期,Ⅷ族(2分) d
(2)角形(或V形)(2分) sp2(2分) 极性(1分)
(3) Si(2分) 2 (2分) (4) 12 (2分)
【解析】
试题分析:根据元素在周期表中的相对位置可知a是H,b是Li,c是C,d是N,e是O,f是F,g是Na,h是Mg,i是Al,j是Si,k是S,l是Cl,m是Ar,n是Cr,o是Fe。
(1)铬元素的原子序数是24,则根据核外电子排布规律可知Cr的基态原子的价电子排布为式3d54s1。元素铁的原子序数是26,在周期表的位置是第四周期第Ⅷ族,属于d区。
(2)S在空气中燃烧产物是SO2,中心S原子含有的孤对电子是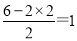 ,所以SO2的分子构型为V形,中心原子的杂化方式为sp2,该分子是非极性分子。
,所以SO2的分子构型为V形,中心原子的杂化方式为sp2,该分子是非极性分子。
(3)第三周期8种元素按单质熔点高低的顺序如左下图,其中序号“8”的元素形成的单质熔点最高,因此该元素是原子晶体硅,元素符号为Si;非金属性越强电负性越大,因此电负性最大的是Cl。由于氯气的熔点仅比Ar高,所以其中电负性最大的是2。
(4)铝是面心立方最紧密堆积,根据晶胞结构可知以立方体的顶点为中心与该顶点距离最近的铝原子共计含有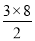 =12个,则晶胞中铝原子的配位数为12。
=12个,则晶胞中铝原子的配位数为12。
考点:考查核外电子排布、元素周期表的结构、元素周期律、电负性、杂化轨道、分子极性以及晶胞结构

 阅读快车系列答案
阅读快车系列答案X、Y、Z、M、W为五种短周期元素。它们在周期表的相对位置如下表:
M | |||||||
X | Y | Z | |||||
W |
则下列说法正确的是:
A.Y、M形成的气态化合物在标准状况下的密度为0.76 g.L-1
B.原子半径:W>Z>Y>X>M
C.由X元素形成的单质一定是原子晶体
D.XZ2、X2M2、W2Z2均为直线型的共价化合物
【化学-选修2:化学与技术】(15分)
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成的。由蛇纹石制取碱式碳酸镁的实验步骤如下:

(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是_ 。
(2)进行Ⅰ操作时,控制溶液的pH=7~8(有关氢氧化物沉淀的pH见下表),则沉淀物A的主要成份为 ,沉淀物B的主要成份为 。
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀的PH值 | 1.5 | 3.3 | 9.4 |
(3)若要从沉淀物A中提取出某种可用于工业冶炼铝的原料,应先向A中加入 溶液(填物质化学式)再过滤,然后向滤液中通入过量CO2,过滤、灼烧。请写出通入CO2时发生反应的离子方程式 。
(4)为确定产品aMgCO3?bMg(OH)2?cH2O中a、b、c的值,称取18.2g样品完全分解后,测得产生6.6gCO2和8.0g MgO,由此可知,产品的化学式中a=______、b=_______、c=______。
下列图中的实验方案,能达到实验目的的是
A | B | C | D | |
实验 方案 |
|
|
|
|
实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 制备Fe(OH)2并能较长时间观察其颜色 | 除去CO2气体中混有的SO2 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
下列离子方程式的书写及评价均合理的是
选项 | 离子方程式 | 评价 |
A | 将2 mol Cl2通入到含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 | 正确; Cl2过量,Fe2+、I-均被氧化 |
B | 用Cu电极电解NaCl溶液阳极的电极反应式: 2Cl--2e-===Cl2↑ | 正确; Cl-优先于OH-放电 |
C | 过量SO2通入到NaClO溶液中: SO2+H2O+ClO-===HClO+HSO3- | 正确; H2SO3的酸性强于HClO |
D | Mg(HCO3)2溶液与足量的NaOH溶液反应: Mg2++2HCO3-+4OH-=== Mg(OH)2 ↓ +2 CO32-+2 H2O | 正确; Mg(OH)2比MgCO3更难溶 |
(本题共14分)合金的性能往往优于组成金属,因而用途非常广泛。钠钾合金可在核反应堆中用作导热剂。5.05g钠钾合金溶于200mL水生成0.075mol氢气。
54.计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
55.计算并确定该钠-钾合金的化学式。
镁铝合金广泛用于火箭、导弹和飞机制造业等。取不同质量的镁铝合金样品分别和30ml相同浓度的盐酸反应,所取合金质量与产生气体体积(标况下)如下表所示:
实验序号 | A | B | C |
合金质量/mg | 510 | 765 | 918 |
气体体积/mL | 560 | 672 | 672 |
56.计算镁铝合金中镁铝的质量之比。
铜锡合金,又称青铜,是人类使用最早的合金。不同的铜锡比例可以产生不同的效用,若含锡量为1/4—1/7(质量比)的青铜被称作重青铜,受敲击时能发出洪亮的声音。
57.现有一铜锡合金样品,可通过至少增加ag铜或至少减少bg锡恰好使其成为钟青铜,且最终得到的钟青铜质量正好相差一半。求原铜锡合金样品中铜锡的物质的量之比。
 键。
键。




 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是