题目内容
(12分)将标准状况下的11.2LNH3溶于100mL,水中,得到密度为O.868g/cm3的氨水。
(1)该气体的物质的量为 mol:溶液的体积为 L;
所得氨水的物质的量浓度为 mol/L。
(2)若取上述氨水30.OmL与70.0mL 2.00mol/L的AlCl3溶液相混合,产生白色沉淀的质量是 g。
(3)若取某浓度的NaOH溶液50.0mL与70.OmL 2.00mol/L的AlCl3溶液相混合,有白色沉淀产生。
测得溶液中铝元素与沉淀中铝元素质量相等,则NaOH溶液的物质的量浓度可能为 mol/L。
(1) 0.5;0.125 ;4
(2) 3.12
(3) 4.2 或9.8 (各2分)

练习册系列答案
相关题目
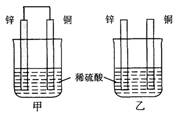
(本题共12分)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
(1)下列说法正确的是____________。
| A.甲、乙均为化学能转变为电能的装置 |
| B.乙中铜片上没有明显变化 |
| C.甲中铜片质量减少、乙中锌片质量减少 |
| D.两烧杯中溶液的c(H+)均增小 |
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为_______________。
(4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为_________________。
(5) 甲中锌片上发生的电极反应: _________________________;
(6) 若甲中两电极的总质量为60 g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为47 g,则:氢气的体积(标准状况)为________。