题目内容
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O═2NO+HNO3+9HF.下列有关该反应的说法正确的是( )
| A、NF3分子中所有原子共平面 |
| B、NF3在反应中既做氧化剂又做还原剂 |
| C、生成0.2mol HNO3时转移0.2mol电子 |
| D、氧化产物与还原产物的物质的量之比为2:1 |
考点:氧化还原反应
专题:
分析:3NF3+5H2O=2NO+HNO3+9HF反应中,只有N元素的化合价发生变化,NF3既是氧化剂又是还原剂,从化合价的变化的角度分析氧化还原反应.
解答:
解:A.N原子上有1对孤对电子,有3个N-F键,类似氨气的结构,则NF3分子中N原子是sp3杂化,分子呈三角锥形,所以所有原子不共平面,故A错误
B.只有N元素的化合价发生变化,NF3既是氧化剂又是还原剂,故B正确;
C.生成0.2molHNO3,转移的电子的物质的量为0.2mol×(5-3)=0.4mol,故C错误;
D.则NO为还原产物,NF3生成NO,被还原,则NO为还原产物,NF3生成HNO3,被氧化,则HNO3为氧化产物,所以氧化产物与还原产物的物质的量之比为1:2,故D错误;
故选B.
B.只有N元素的化合价发生变化,NF3既是氧化剂又是还原剂,故B正确;
C.生成0.2molHNO3,转移的电子的物质的量为0.2mol×(5-3)=0.4mol,故C错误;
D.则NO为还原产物,NF3生成NO,被还原,则NO为还原产物,NF3生成HNO3,被氧化,则HNO3为氧化产物,所以氧化产物与还原产物的物质的量之比为1:2,故D错误;
故选B.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素化合价的升降为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,注意从化合价的角度分析,题目难度不大.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案
相关题目
下列叙述正确的是( )
| A、1mol氧的质量为16g?mol-1 |
| B、H2O的摩尔质量为18g |
| C、22.4LH2的物质的量为1 mol |
| D、CO和N2的摩尔质量相等 |
下列说法正确的是( )
| A、由非金属元素组成的化合物不一定是共价化合物 |
| B、X2+的核外电子数目为18,则X在第三周期ⅡA族 |
| C、HF很稳定是因为其分子间能形成氢键 |
| D、同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
下列有机物结构、性质相关的叙述正确的是( )
| A、苯的硝化、酯化反应均可看作取代反应 |
| B、乙酸、乙酸乙酯互为同分异构体 |
| C、乙醇和乙酸分子中都含有羟基,它们都能和氢氧化钠反应生成H2O |
| D、糖类、油脂和蛋白质都能发生水解,充分燃烧的产物都是CO2和H2O |
下列化合物中,既含有离子键又含有共价键的是( )
| A、NH4Cl |
| B、CO2 |
| C、NaCl |
| D、HCl |
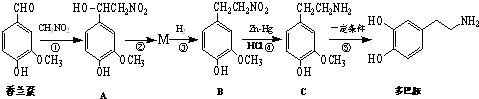
 )是生物体中重要的生物碱.写出用苯甲醇、硝基甲烷为原料制备苯乙胺的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
)是生物体中重要的生物碱.写出用苯甲醇、硝基甲烷为原料制备苯乙胺的合成路线流程图(无机试剂任选).合成路线流程图示例如下: