题目内容
14.下列说法中正确的是( )| A. | 有化学键断裂或化学键形成的过程都是化学变化 | |
| B. | Na2O2和Na2O都属于碱性氧化物 | |
| C. | 溶液中的溶质粒子能透过滤纸,而胶体中的分散质粒子不能透过滤纸,所以可以用滤纸来分离溶液和胶体 | |
| D. | 食盐溶液能导电,但食盐溶液不是电解质 |
分析 A.化学变化中一定伴随化学键的断裂和生成;
B.与酸反应生成盐和水的金属氧化物为碱性氧化物;
C.胶体粒子、溶液均可透过滤纸;
D.电解质必须为化合物.
解答 解:A.化学变化中一定伴随化学键的断裂和生成,则有化学键断裂和化学键形成的过程都是化学变化,故A错误;
B.与酸反应生成盐和水的金属氧化物为碱性氧化物,则Na2O属于碱性氧化物,而Na2O2不是,故B错误;
C.胶体粒子、溶液均可透过滤纸,则过滤不能分离,故C错误;
D.电解质必须为化合物,而食盐溶液为溶液,导电与自由电子有关,食盐溶液既不是电解质也不是非电解质,故D正确;
故选D.
点评 本题考查物质分类及化学变化等,为高频考点,把握碱性氧化物、混合物分离提纯、化学变化的实质为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.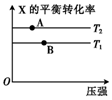 向某密闭容器中充入1mol X与2mol Y发生反应:X(g)+2Y(g)?aZ(g)△H<0,达到平衡后,改变某一条件(温度或容器体积),X的平衡转化率的变化如图所示.下列说法中正确的是( )
向某密闭容器中充入1mol X与2mol Y发生反应:X(g)+2Y(g)?aZ(g)△H<0,达到平衡后,改变某一条件(温度或容器体积),X的平衡转化率的变化如图所示.下列说法中正确的是( )
 向某密闭容器中充入1mol X与2mol Y发生反应:X(g)+2Y(g)?aZ(g)△H<0,达到平衡后,改变某一条件(温度或容器体积),X的平衡转化率的变化如图所示.下列说法中正确的是( )
向某密闭容器中充入1mol X与2mol Y发生反应:X(g)+2Y(g)?aZ(g)△H<0,达到平衡后,改变某一条件(温度或容器体积),X的平衡转化率的变化如图所示.下列说法中正确的是( )| A. | a=2 | B. | T2>T1 | ||
| C. | A点的反应速率:3v正(X)=v逆(Z) | D. | 表示A、B两点的反应速率:v(A)>v(B) |
2.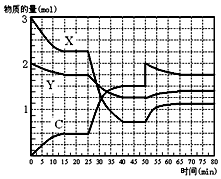 如图表示在一定条件下的1L的密闭容器中,X、Y、C三种气体因发生反应,三种气体的物质的量随时间的变化情况.下表是3mol X和1mol Y在一定温度和一定压强下反应,达到平衡时C的体积分数(C%).
如图表示在一定条件下的1L的密闭容器中,X、Y、C三种气体因发生反应,三种气体的物质的量随时间的变化情况.下表是3mol X和1mol Y在一定温度和一定压强下反应,达到平衡时C的体积分数(C%).
①X、Y、C三种气体发生反应的化学方程式为Y+3X?2C.
②表中a的取值范围是25.1<a<64.2.
③根据上图和上表分析,25min~40min内图中曲线发生变化的原因可能是缩小容器体积或增大压强.
 如图表示在一定条件下的1L的密闭容器中,X、Y、C三种气体因发生反应,三种气体的物质的量随时间的变化情况.下表是3mol X和1mol Y在一定温度和一定压强下反应,达到平衡时C的体积分数(C%).
如图表示在一定条件下的1L的密闭容器中,X、Y、C三种气体因发生反应,三种气体的物质的量随时间的变化情况.下表是3mol X和1mol Y在一定温度和一定压强下反应,达到平衡时C的体积分数(C%).| 压强/Mpa C% 温度/℃ | 0.1 | 10 | 20 |
| 200 | 15.3 | 81.5 | 86.4 |
| 300 | 2.2 | a | 64.5 |
| 400 | 0.4 | 25.1 | 38.2 |
| 500 | 0.1 | 10.6 | 19.1 |
②表中a的取值范围是25.1<a<64.2.
③根据上图和上表分析,25min~40min内图中曲线发生变化的原因可能是缩小容器体积或增大压强.
19.下列反应中,反应后固体物质增重的是( )
| A. | 氢气通过灼热的CuO粉末 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 将Na2O2投入水中 | D. | 将锌粒投入Cu(NO3)2溶液 |
6.下列有关说法正确的是( )
| A. | 漂白粉、氨水和冰醋酸都属于混合物 | |
| B. | Fe(OH)3胶体无色、透明,能产生丁达尔现象 | |
| C. | 淀粉、纤维素、天然橡胶都是天然高分子化合物 | |
| D. | SiO2既能和NaOH溶液反应又能和氢氟酸反应,所有是两性氧化物 |
3.下列化学方程式或离子方程式正确的是( )
| A. | 小苏打溶液与过量的澄清石灰水反应:Ca2++OH-+HCO${\;}_{3}^{-}$=CaCO3↓+H2O | |
| B. | 少量SO2通入氢氧化钠溶液中:OH-+SO2=HSO${\;}_{3}^{-}$ | |
| C. | 双氧水作脱氯剂,用于消除水中的氯气:Cl2+H2O2=2HCl+O2 | |
| D. | Fe3O4溶于氢碘酸的离子方程式:Fe3O4+8H+=2Fe3++Fe2++4H2O |
4.化学与生活和生产密切相关,下列过程未涉及到化学变化的是( )
| A. | 皮肤被紫外线灼伤 | B. | NaHCO3药片做抗酸药 | ||
| C. | 甘油做护肤保湿剂 | D. | 供能剂MgH2为氢能源汽车提供H2 |
 ,水玻璃可用作木材防火剂,其主要成分是(写化学式)Na2SiO3.写出工业生产粗硅的化学方程式SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.高温条件下,二氧化硅、碳粉、氮气以物质的量之比3:6:2反应可以生成氮化硅陶瓷(一种新型无机非金属材料,具有耐高温、耐磨、抗氧化等特性)和另一种气体化合物,该反应的化学方程式为3SiO2+2N2+6C $\frac{\underline{\;高温\;}}{\;}$Si3N4+6CO.
,水玻璃可用作木材防火剂,其主要成分是(写化学式)Na2SiO3.写出工业生产粗硅的化学方程式SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.高温条件下,二氧化硅、碳粉、氮气以物质的量之比3:6:2反应可以生成氮化硅陶瓷(一种新型无机非金属材料,具有耐高温、耐磨、抗氧化等特性)和另一种气体化合物,该反应的化学方程式为3SiO2+2N2+6C $\frac{\underline{\;高温\;}}{\;}$Si3N4+6CO.