题目内容
升高温度,下列数据不一定增大的是( )
| A、电离平衡常数Ka |
| B、水解平衡常数Kb |
| C、化学平衡常数K |
| D、水的离子积常数Kw |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、弱电解质的电离是吸热过程,升高温度促进弱电解质的电离,电离平衡常数增大;
B、水解过程是吸热反应,升高温度促进水解;
C、若正反应为放热反应,升高温度平衡向吸热反应方向移动,化学平衡常数减小;
D、水的电离过程是吸热的,升高温度促进水的电离.
B、水解过程是吸热反应,升高温度促进水解;
C、若正反应为放热反应,升高温度平衡向吸热反应方向移动,化学平衡常数减小;
D、水的电离过程是吸热的,升高温度促进水的电离.
解答:
解:A、弱电解质的电离是吸热过程,升高温度促进弱电解质的电离,电离平衡常数增大,故A不选;
B、水解过程是吸热反应,升高温度促进水解,水解平衡常数Kb增大,故B不选;
C、若正反应为放热反应,升高温度平衡向吸热反应方向移动,化学平衡常数减小,故C选;
D、水的电离过程是吸热的,升高温度促进水的电离,升高温度电离程度增大,水的离子积增大,故D不选;
故选C.
B、水解过程是吸热反应,升高温度促进水解,水解平衡常数Kb增大,故B不选;
C、若正反应为放热反应,升高温度平衡向吸热反应方向移动,化学平衡常数减小,故C选;
D、水的电离过程是吸热的,升高温度促进水的电离,升高温度电离程度增大,水的离子积增大,故D不选;
故选C.
点评:本题考查温度对反应速率的影响、温度对化学平衡常数与水的离子积以及电离平衡常数的影响,比较基础,注意基础知识的掌握.

练习册系列答案
相关题目
下列物质的分离方法不正确的是( )
| A、用过滤的方法除去食盐中泥沙 |
| B、用蒸馏的方法将海水淡化 |
| C、用酒精萃取碘水中的碘单质 |
| D、用加热的方法除去碳酸钠中的碳酸氢钠 |
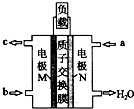 甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇 燃料电池的总反应式2CH40+302=2C02↑+4H20,如图是该燃料电池的示意图.下列说法错误的是( )
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇 燃料电池的总反应式2CH40+302=2C02↑+4H20,如图是该燃料电池的示意图.下列说法错误的是( )| A、燃料电池将化学能转化为电能 |
| B、a是甲醇,b是氧气 |
| C、质子从M电极区穿过交换膜移向N电极区 |
| D、负极反应:CH40-6e-+H20=C02↑+6H+ |
25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是( )
| A、向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| B、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| C、向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D、将水加热,Kw增大,pH不变 |