题目内容
铝及其化合物在工业生产、日常生活中有广泛用途.
(l)工业上冶炼铝需要冰晶石(Na3AlF6)是 (填“离子化合物”或“共价化合物”).工业上,利用氢氟酸和碳酸钠、氢氧化铝反应制备冰晶石.理论上,参与反应的HF、Na2CO3、Al(OH)3的物质的量之比为 .
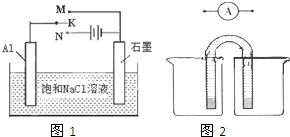
(2)工业制备铝,用石墨作电极,写出阴极反应式: ,阳极上收集的氧气体积小于理论值,可能的原因是 .
(3)铝热反应是工业冶炼难熔金属的重要反应.
①Al(s)+
O2(g)═
Al2O3(s)△H1
②4V(s)+5O2(g)═2V2O5(s)△H2
3V2O5(s)+10Al(s)═5Al2O3(s)+6V(s)△H= .
(4)铁明矾化学式为Al2Fe(SO4)4,它是一种净水剂.在铁明矾溶液中
(填“>”、“<”或“=”).
(l)工业上冶炼铝需要冰晶石(Na3AlF6)是
(2)工业制备铝,用石墨作电极,写出阴极反应式:
(3)铝热反应是工业冶炼难熔金属的重要反应.
①Al(s)+
| 3 |
| 4 |
| 1 |
| 2 |
②4V(s)+5O2(g)═2V2O5(s)△H2
3V2O5(s)+10Al(s)═5Al2O3(s)+6V(s)△H=
(4)铁明矾化学式为Al2Fe(SO4)4,它是一种净水剂.在铁明矾溶液中
| c(Al3+) | ||
c(
|
| 1 |
| 2 |
考点:电解原理,化学方程式的有关计算,用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化,化学平衡专题,电化学专题
分析:(1)Na3AlF6是由活泼金属与活泼非金属构成的;根据原子守恒计算;
(2)电解熔融的氧化铝,阴极上铝离子得电子,阳极上氧离子失电子,高温下C与氧气反应;
(3)根据盖斯定律结合已知热化学方程式计算;
(4)铝离子水解,铝离子浓度减小.
(2)电解熔融的氧化铝,阴极上铝离子得电子,阳极上氧离子失电子,高温下C与氧气反应;
(3)根据盖斯定律结合已知热化学方程式计算;
(4)铝离子水解,铝离子浓度减小.
解答:
解:(1)Na3AlF6是由活泼金属Na、Al与活泼非金属F构成的,微粒之间以静电作用结合,属于离子键,是离子化合物已知冰晶石的化学式:Na3AlF6,令Na3AlF6为1mol,则需要HF6mol,Na2CO3
mol,Al(OH)32mol,则理论上,参与反应的HF、Na2CO3、Al(OH)3的物质的量之比为12:3:2;
故答案为:离子化合物;12:3:2;
(2)电解熔融的氧化铝,阴极上铝离子得电子,其电极反应式为:Al3++3e-=Al,阳极上氧离子失电子,高温下C与氧气反应,所以阳极上收集的氧气体积小于理论值;
故答案为:Al3++3e-=Al;高温下氧气与石墨反应;
(3)已知①Al(s)+
O2(g)═
Al2O3(s)△H1
②4V(s)+5O2(g)═2V2O5(s)△H2
由盖斯定律:①×10-②×
得 3V2O5(s)+10Al(s)═5Al2O3(s)+6V(s)△H=
,
故答案为:
;
(4)在铁明矾溶液中铝离子水解,铝离子浓度减小,硫酸根离子的浓度不变,所以溶液中
<
,
故答案为:<.
| 3 |
| 2 |
故答案为:离子化合物;12:3:2;
(2)电解熔融的氧化铝,阴极上铝离子得电子,其电极反应式为:Al3++3e-=Al,阳极上氧离子失电子,高温下C与氧气反应,所以阳极上收集的氧气体积小于理论值;
故答案为:Al3++3e-=Al;高温下氧气与石墨反应;
(3)已知①Al(s)+
| 3 |
| 4 |
| 1 |
| 2 |
②4V(s)+5O2(g)═2V2O5(s)△H2
由盖斯定律:①×10-②×
| 3 |
| 2 |
| 20△H1-3△H2 |
| 2 |
故答案为:
| 20△H1-3△H2 |
| 2 |
(4)在铁明矾溶液中铝离子水解,铝离子浓度减小,硫酸根离子的浓度不变,所以溶液中
| c(Al3+) | ||
c(
|
| 1 |
| 2 |
故答案为:<.
点评:本题考查了离子化合物的概念、电解原理的应用、盖斯定律的应用、盐的水解原理的应用等,题目侧重于反应原理的应用的考查,题目难度中等.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
下列说法不正确的是( )
| A、汽车尾气中的氮氧化物与光化学烟雾形成有关 |
| B、电解氯化铝溶液可获得金属铝 |
| C、大量燃烧含硫燃料是形成酸雨的主要原因 |
| D、铜具有良好的导电性,常用来制作印刷电路板 |
四种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子核质子数之比为1:2,X和Y的电子数之差为4.下列说法正确的是( )
| A、原子半径大小:Z>Y>X>W |
| B、W、Y、Z中最简单氢化物稳定性最弱的是W |
| C、Z元素单质在化学反应中只表现氧化性 |
| D、z元素氧化物对应水化物的酸性一定强于Y |
下列说法正确的是( )
A、若完全燃烧,1mol雄酮(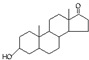 )比雌酮( )比雌酮( )多消耗3mol O2 )多消耗3mol O2 |
| B、正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高 |
| C、蔗糖、麦芽糖和乳糖的分子式都为C12H22O11,均能发生银镜反应 |
| D、乙醇依次通过消去、取代、加成反应可生成乙二醇 |
 如图某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用硫酸钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔知滤纸上写“嫦娥奔月”,会出现红色字迹,据此下列叙述正确的是( )
如图某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用硫酸钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔知滤纸上写“嫦娥奔月”,会出现红色字迹,据此下列叙述正确的是( )| A、铅笔端作阴极,铂片端发生还原反应 |
| B、铅笔端有少量钠生成 |
| C、硫酸钠溶液不可用硝酸钾溶液代替 |
| D、铂片端发生的电极反应为:40H--4e-=2H2O+O2↑ |
 以下是一些物质的熔沸点数据(常压):
以下是一些物质的熔沸点数据(常压):