题目内容
(10分)ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.
(1)工业上可以通过下列方法制取ClO2,请完成该化学反应方程式: 2KClO3+SO2=2ClO2+________。
(2)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O32-+I2=S4O62-+2I-)
Ⅲ.加硫酸调节水样pH至1~3。操作时,不同pH环境中粒子种类如下图所示:
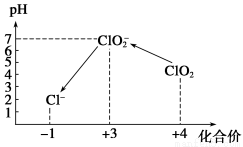
请回答:
①操作Ⅰ中反应的离子方程式是______________________________。
②确定操作Ⅱ完全反应的现象是______________________________。
③在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是__________________。
④若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol·L-1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是________mg·L-1。
(1)K2SO4 (2分)
(2)①2ClO2+2I-=2ClO +I2 (2分);②蓝色消失,半分钟内不变色(2分);
+I2 (2分);②蓝色消失,半分钟内不变色(2分);
③ClO +4I-+4H+=Cl-+2I2+2H2O(2分);④0.675(2分)
+4I-+4H+=Cl-+2I2+2H2O(2分);④0.675(2分)
【解析】
试题分析:(1)工业上可以通过KClO3与SO2发生氧化还原反应产生ClO2,根据氧化还原反应中电子转移数目相等及质量守恒定律,可知该化学反应方程式是: 2KClO3+SO2=2ClO2+K2SO4;①操作Ⅰ中ClO2将I-氧化为I2,反应的离子方程式是2ClO2+2I-=2ClO +I2; ②操作Ⅱ完全反应时溶液中的I2反应完全,因此溶液的颜色由蓝色变为无色,且半分钟内不变色;③在操作Ⅲ过程中,溶液又呈蓝色,是由于ClO
+I2; ②操作Ⅱ完全反应时溶液中的I2反应完全,因此溶液的颜色由蓝色变为无色,且半分钟内不变色;③在操作Ⅲ过程中,溶液又呈蓝色,是由于ClO 在碱性环境中将I-又氧化为I2,I2遇淀粉变蓝色,反应的离子方程式是ClO
在碱性环境中将I-又氧化为I2,I2遇淀粉变蓝色,反应的离子方程式是ClO +4I-+4H+=Cl-+2I2+2H2O;④根据反应方程式可得关系式是:2ClO2~I2~2S2O32-。n(S2O32-)= 1.0×10-3 mol/L × 0.01L=1.0×10-5mol;所以n(ClO2)= 1.0×10-5mol;m(ClO2)= 1.0×10-5mol×67. 5×103mg/mol=0.675mg;若水样的体积为1.0 L,所以水样中ClO2的浓度是0.675mg÷1L =0.675mg/L。
+4I-+4H+=Cl-+2I2+2H2O;④根据反应方程式可得关系式是:2ClO2~I2~2S2O32-。n(S2O32-)= 1.0×10-3 mol/L × 0.01L=1.0×10-5mol;所以n(ClO2)= 1.0×10-5mol;m(ClO2)= 1.0×10-5mol×67. 5×103mg/mol=0.675mg;若水样的体积为1.0 L,所以水样中ClO2的浓度是0.675mg÷1L =0.675mg/L。
考点:考查氧化还原反应方程式的配平、滴定终点的判断、关系式法在化学计算中的应用的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案



 D.(n-m)×a%
D.(n-m)×a%