题目内容
下列电子式书写错误的是( )
A、 |
B、 |
C、 |
D、Na+ |
考点:电子式
专题:化学用语专题
分析:在元素符号周围用“?”和“×”来表示原子的最外层电子(价电子),这种式子叫做电子式.
首先判断物质的成键类型,是由离子键还是共价键形成的物质.
1.原子的电子式:
由于中性原子既没有得电子,也没有失电子,所以书写电子式时应把原子的最外层电子全部排列在元素符号周围.排列方式为在元素符号上、下、左、右四个方向,每个方向不能超过2个电子;
2.金属阳离子的电子式:
金属原子在形成阳离子时,最外层电子已经失去,但电子式仅画出最外层电子,所以在画阳离子的电子式时,就不再画出原最外层电子,但离子所带的电荷数应在元素符号右上角标出.所以金属阳离子的电子式即为离子符号;
3.非金属阴离子的电子式:
一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些电子都应画出,并将符号用“[]”括上,右上角标出所带的电荷数,电荷的表示方法同于离子符号;
4.共价化合物的电子式:
共价化合物是原子间通过共用电子对结合而成的.书写时将共用电子对画在两原子之间,每个原子的未成对电子和孤对电子也应画出.因不同元素原子吸引电子能力不同,则共用电子对偏向吸引电子能力强的原子,而偏离吸引电子能力弱的原子;
5.根离子的电子式:
根离子中,若不同原子间以共价键结合,画法同共价化合物,因根离子带有电荷,所以应把符号用“[]”括起来,右上角标出电荷数.例如,铵根阳离子;氢氧根离子;
6.离子化合物的电子式:
先根据离子电子式的书写方法,分别画出阴、阳离子的电子式,然后让阴、阳离子间隔排列,注意相同离子不能合并.
首先判断物质的成键类型,是由离子键还是共价键形成的物质.
1.原子的电子式:
由于中性原子既没有得电子,也没有失电子,所以书写电子式时应把原子的最外层电子全部排列在元素符号周围.排列方式为在元素符号上、下、左、右四个方向,每个方向不能超过2个电子;
2.金属阳离子的电子式:
金属原子在形成阳离子时,最外层电子已经失去,但电子式仅画出最外层电子,所以在画阳离子的电子式时,就不再画出原最外层电子,但离子所带的电荷数应在元素符号右上角标出.所以金属阳离子的电子式即为离子符号;
3.非金属阴离子的电子式:
一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些电子都应画出,并将符号用“[]”括上,右上角标出所带的电荷数,电荷的表示方法同于离子符号;
4.共价化合物的电子式:
共价化合物是原子间通过共用电子对结合而成的.书写时将共用电子对画在两原子之间,每个原子的未成对电子和孤对电子也应画出.因不同元素原子吸引电子能力不同,则共用电子对偏向吸引电子能力强的原子,而偏离吸引电子能力弱的原子;
5.根离子的电子式:
根离子中,若不同原子间以共价键结合,画法同共价化合物,因根离子带有电荷,所以应把符号用“[]”括起来,右上角标出电荷数.例如,铵根阳离子;氢氧根离子;
6.离子化合物的电子式:
先根据离子电子式的书写方法,分别画出阴、阳离子的电子式,然后让阴、阳离子间隔排列,注意相同离子不能合并.
解答:
解:A.CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ,故A错误;
,故A错误;
B.HCl属于共价化合物,不存在离子键,分子中氢原子与氯原子之间形成1对共用电子对,HCl电子式为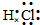 ,故B正确;
,故B正确;
C.氢氧根是原子团阴离子,要用中括号括起来,并在右上角表明电荷数,故C正确;
D.氯化钠为离子化合物,其电子式中需要标出阴阳离子所带电荷,氯化钠的电子式为: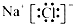 ,故D正确.
,故D正确.
故选A.
 ,故A错误;
,故A错误; B.HCl属于共价化合物,不存在离子键,分子中氢原子与氯原子之间形成1对共用电子对,HCl电子式为
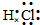 ,故B正确;
,故B正确;C.氢氧根是原子团阴离子,要用中括号括起来,并在右上角表明电荷数,故C正确;
D.氯化钠为离子化合物,其电子式中需要标出阴阳离子所带电荷,氯化钠的电子式为:
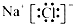 ,故D正确.
,故D正确.故选A.
点评:本题考查常用化学用语的书写,难度较小,注意:①阴离子的电子式要用[]括起来并在右上角标明电荷,阳离子的电子式除铵离子外,一般与阳离子符号相同;②注意4类电子式:阳离子的电子式、阴离子的电子式、原子的电子式、分子的电子式;③做题时要特别注意看清要求是“写出化合物的电子式”还是“用电子式表示化合物的形成过程”.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
下列关于SiO2的说法不正确的是( )
| A、不能与水直接化合生成相应的酸 |
| B、能与强碱溶液反应生成盐和水 |
| C、高纯度的SiO2可以用来制半导体芯片 |
| D、可以被氢氟酸腐蚀 |
无论在酸性还是碱性溶液中,都能大量共存的离子组是( )
A、Na+、K+、HCO
| ||||
B、Na+、Cu2+、SO
| ||||
| C、Br -、Ba2+、Cl-、K+ | ||||
D、Ca2+、K+、CO
|
将少量CO2分别通入①CaCl2溶液,②Na2SiO3溶液,③Ca(ClO)2溶液,④Ba(OH)2溶液,有沉淀析出的是( )
| A、①②③④ | B、①②④ |
| C、②③④ | D、①③ |
下列有关说法中正确的是( )
| A、有单质生成的反应一定是置换反应 |
| B、焰色反应是元素表现出来的化学性质 |
| C、由两种元素组成,原子个数比为1:1的物质一定是纯净物 |
| D、能与酸反应产物中有盐和水的氧化物不一定是碱性氧化物 |
下列各组中两个溶液间的反应,均可用同一离子方程式表示的是( )
| A、HCl和Na2CO3与HCl和NaHCO3 |
| B、AgNO3和HCl与AgNO3和H2SO4 |
| C、BaCl2和Na2SO4 与Ba(OH)2和CuSO4 |
| D、KOH和CuCl2与Ba(OH)2和CuCl2 |
一定温度下,将少量生石灰放入一定量的饱和石灰水中,搅拌并冷却到原温度,下列说法正确的是( )
| A、溶质的质量增大 |
| B、溶质的物质的量浓度增大 |
| C、Ca(OH)2浓度不变 |
| D、溶质的质量分数增大 |
化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是( )
| A、塑料袋在全球“失宠”,是因为塑料袋填埋占用土地,且难以降解 |
| B、举行“地球一小时”熄灯活动,会影响经济发展及社会生活,所以不宜推广 |
| C、有色玻璃是某些胶态金属分散于玻璃中制成的胶体 |
| D、太阳能是目前人类生产生活直接利用的、转化效率最高的能源 |