题目内容
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
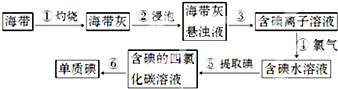
已知:四氯化碳沸点是76.8℃,碘单质的沸点是184.35℃.
请填写下列空白:
(1)步骤③的实验操作名称是 ;步骤⑤的实验操作名称是 ;
(2)步骤⑤操作所需的玻璃仪器主要是 (填仪器名称).该操作过程中,可供选择的有机溶剂是 .A.酒精B.四氯化碳C.煤油D.水
(3)检验提取碘后的水溶液中是否还含有单质碘,可选用的试剂是 .

已知:四氯化碳沸点是76.8℃,碘单质的沸点是184.35℃.
请填写下列空白:
(1)步骤③的实验操作名称是
(2)步骤⑤操作所需的玻璃仪器主要是
(3)检验提取碘后的水溶液中是否还含有单质碘,可选用的试剂是
考点:海水资源及其综合利用
专题:化学应用
分析:(1)分离固体和液体用过滤,将碘水转化为含碘的有机溶液,需用对卤素单质溶解能力强的有机溶剂把碘从碘水中提取出来,对应进行的实验操作是萃取;
(2)把碘从碘水中提取出来,对应进行的实验操作是萃取,需要的是分液漏斗;利用碘易溶于有机溶剂的性质来进行提取,须注意:选择的能提取碘的试剂除了对I2有强的溶解能力处,还必须难溶于水,否则不能进行分液分离;
(3)碘遇淀粉变蓝色.
(2)把碘从碘水中提取出来,对应进行的实验操作是萃取,需要的是分液漏斗;利用碘易溶于有机溶剂的性质来进行提取,须注意:选择的能提取碘的试剂除了对I2有强的溶解能力处,还必须难溶于水,否则不能进行分液分离;
(3)碘遇淀粉变蓝色.
解答:
解:(1)将悬浊液分离为残渣和含碘离子溶液应选择过滤的方法.将碘水转化为含碘的有机溶液,需用对卤素单质溶解能力强的有机溶剂把碘从碘水中提取出来,对应进行的实验操作是萃取,步骤③的实验操作名称是过滤,步骤⑤的实验操作名称是萃取分液;
故答案为:过滤;萃取分液;
(2)把碘从碘水中提取出来,对应进行的实验操作是萃取,需要的是分液漏斗;利用碘易溶于有机溶剂的性质来进行提取,须注意:选择的能提取碘的试剂除了对I2有强的溶解能力处,还必须难溶于水,否则不能进行分液分离,符合条件的是四氯化碳和煤油;
故答案为:分液漏斗,BC;
(3)根据淀粉遇碘变蓝色检验碘单质的存在,实验操作为取少量提取碘后的水溶液于试管中,加入几滴淀粉试液;观察是否出现蓝色(如果变蓝,说明还有单质碘),故答案为:淀粉;
故答案为:过滤;萃取分液;
(2)把碘从碘水中提取出来,对应进行的实验操作是萃取,需要的是分液漏斗;利用碘易溶于有机溶剂的性质来进行提取,须注意:选择的能提取碘的试剂除了对I2有强的溶解能力处,还必须难溶于水,否则不能进行分液分离,符合条件的是四氯化碳和煤油;
故答案为:分液漏斗,BC;
(3)根据淀粉遇碘变蓝色检验碘单质的存在,实验操作为取少量提取碘后的水溶液于试管中,加入几滴淀粉试液;观察是否出现蓝色(如果变蓝,说明还有单质碘),故答案为:淀粉;
点评:本题考查制备实验方案的设计,题目难度中等,注意基本实验操作的要点和注意事项.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列有关实验的叙述正确的是( )
| A、除去水中的Na+、SO42-、Cl-等杂质可用蒸馏的方法 |
| B、除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
| C、用铂丝蘸取少量某溶液进行焰色反应,若火焰呈黄色,则原溶液含有钠盐 |
| D、某溶液加入盐酸酸化的BaCl2溶液,若有白色沉淀生成,则原溶液含有SO42- |
在标准状况下将1.92g铜粉投入一定量浓HNO3中随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混和气体1.12L,则混和气体中NO的体积为( )
| A、112mL |
| B、1008mL |
| C、224mL |
| D、336mL |
下列说法正确的是( )
| A、符合CnH2n+2通式的一定是同系物 |
| B、符合CnH2n通式的一定是同系物 |
| C、符合CnH2n-2通式的一定是同系物 |
| D、符合CnH2n-6通式的一定是同系物 |