题目内容
下列说法正确的是( )
A.HClO中氯元素化合价比HClO4中氯元素化合价低,所以,HClO4的氧化性强
B.已知①Fe + Cu2+ = Fe2+ + Cu;② 2Fe3+ + Cu = 2Fe2+ + Cu2+,则氧化性强弱顺序为:Fe3+ > Cu2+> Fe2+
C.已知还原性:B- > C-> D-,反应 2C- + D2 = 2D- +C2和反应 2C-+ B2 = 2B-+C2都能发生
D.具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应
B
【解析】
试题分析:A.物质的氧化性的强弱与元素的化合价的高低无直接的关系,错误;B.物质的氧化性:氧化剂>氧化产物。①Fe + Cu2+ = Fe2+ + Cu中氧化性Cu2+> Fe2+;② 2Fe3++Cu =2Fe2++Cu2+中氧化性Fe3+ > Cu2+;所以氧化性强弱顺序为:Fe3+ > Cu2+> Fe2+,正确;C.还原性强的物质能够发生反应制取还原性弱的物质,由于还原性:C-> D-,反应 2C-+ D2 = 2D-+C2可以发生;由于还原性:B- > C-,所以反应 2C-+ B2 = 2B-+C2不能发生,错误;D.具有强氧化性和强还原性的物质放在一起在一定条件下才能发生氧化还原反应,错误。
考点:考查氧化还原反应中氧化性、还原性强弱的比较的知识。

(15分)
(1)人们常用催化剂来选择反应进行的方向。下图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。
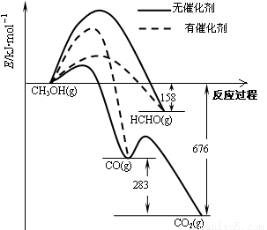
①在有催化剂作用下,CH3OH与O2反应主要生成 (填“CO、CO2” 或“HCHO”)。2HCHO(g)+O2(g)=2CO(g)+2H2O(g) △H= 。
②甲醇制取甲醛可用Ag作催化剂,含有AgCl会 影响Ag催化剂的活性。用氨水可以溶解除去其中的AgCl,写出该反应的离子方程式: 。
(2)已知:CO(g)+ 2H2(g)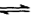 CH3OH(g)△H = -a kJ?mol-1。
CH3OH(g)△H = -a kJ?mol-1。
①经测定不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4 mol·L-1、c(H2)=0.4 mol·L-1、c(CH3OH)=0.8 mol·L-1, 则此时v正 v逆(填“>”、“<”或“=”)。
②某温度下,在体积固定的2L的密闭容器中将1 mol CO和2 mol H2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则0~15 min,用H2表示的平均反应速率为 ,达到平衡时CO的转化率为 。
(3)利用钠碱循环法可除去SO2,消除SO2对环境的污染。吸收液吸收SO2的过程中,pH随n(SO3?-)∶n(HSO3-)变化关系如下表:
n(SO3?-) ∶n(HSO3-) | 91∶9 | 1∶1 | 1∶91 |
pH | 8.2 | 7.2 | 6.2 |
根据上表判断NaHSO3溶液显 性。
② 在NaHSO3溶液中离子浓度关系正确的是 (填字母)。
a. c(Na+)> c(HSO3-)> c(H+)> c(SO32-)> c(OH-)
b. c(Na+)= 2c(SO32-)+ c(HSO3-)
c. c(H2SO3)+ c(H+)= c(SO32-)+ (OH-)
d. c( Na+)+ c(H+)= c(SO32-)+ c(HSO3-)+ c(OH-)
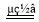 H2↑+ Cl2↑
H2↑+ Cl2↑
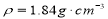 )配制 1mol/L的稀硫酸100mL,按配制溶液时仪器的选用顺序排列,选择正确的是( )
)配制 1mol/L的稀硫酸100mL,按配制溶液时仪器的选用顺序排列,选择正确的是( )