题目内容
(8分:每空2分)将镁、铝的混合物共0.2 mol, 溶于200 mL 4 mol·L—1的盐酸溶液中,然后再滴加2mol·L—1的NaOH溶液。请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量m 随加入NaOH溶液的体积V变化情况如图所示。当V1=160 mL时,则金属粉末中n (Al)= mol;

(2)0~V1段发生的反应的离子方程式为 ;
(3)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+ 刚好沉淀完全,则 滴入NaOH溶液的体积
V(NaOH)= mL;
(4)若镁、铝的混合物仍为0.2 mol,其中镁粉的物质的量分数为a, 改用200 mL 4mol·L—1的硫酸溶解此混合物后,再加入840mL 2 mol·L—1的NaOH溶液,所得沉淀中无Al(OH)3,则a的取值范围为 。
(1)0.08 (2)H++OH-=H2O (3)400 (4)0.6≤a<1
【解析】
试题分析:(1)当V1=160mL时,此时,溶液是MgCl2、AlCl3和NaCl的混合液,由Na+离子守恒可知,
n(NaCl)=n(Na+)=n(NaOH)=0.16L×2mol/L=0.32mol,200mL 4mol/L的盐酸溶液中含有氯化氢的物质的量为:4mol/L×0.2L=0.8mol,设混合物中含有MgCl2xmol、AlCl3为ymol,则:
根据Mg原子、Al原子守恒有:x+y=0.2,
根据Cl-离子守恒有:2x+3y=0.8-0.32=0.48,
联立方程解得:x=0.12、y=0.08,
所以金属粉末中:n(Mg)=0.12mol、n(Al)=y=0.08mol;
(2)0~V1段,滴入氢氧化钠溶液后没有生成沉淀,说明盐酸过量,滴入的氢氧化钠与盐酸反应生成氯化钠和水,反应的离子方程式为:H++OH-=H2O;(3)当溶液中Mg2+、Al3+恰好沉淀完全时,此时,溶液中溶质只有NaCl,根据Cl-离子和Na+离子守恒有:n(Na+)=n(NaCl)=n(HCl)=4mol/L×0.2L=0.8mol,所以需要加入氢氧化钠溶液体积为:V(NaOH)=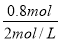 =0.4L=400mL;(4)由于为金属混合物,则a<1,Al的物质的量为:0.1×(1-a)mol,反应后的混合溶液再加入840mL 2mol/L的NaOH溶液,所得沉淀中无Al(OH)3,则溶质为硫酸钠、偏铝酸钠,根据铝元素守恒可知:n(NaAlO2)=0.1×(1-a)mol,根据钠离子守恒,应满足:n(NaOH)≥2n(Na2SO4)+n(NaAlO2),即0.84×2≥2×0.2×4+0.1×(1-a),解得:a≥0.6,所以a的取值范围为:0.6≤a<1。
=0.4L=400mL;(4)由于为金属混合物,则a<1,Al的物质的量为:0.1×(1-a)mol,反应后的混合溶液再加入840mL 2mol/L的NaOH溶液,所得沉淀中无Al(OH)3,则溶质为硫酸钠、偏铝酸钠,根据铝元素守恒可知:n(NaAlO2)=0.1×(1-a)mol,根据钠离子守恒,应满足:n(NaOH)≥2n(Na2SO4)+n(NaAlO2),即0.84×2≥2×0.2×4+0.1×(1-a),解得:a≥0.6,所以a的取值范围为:0.6≤a<1。
考点:考查有关混合物反应的计算。

已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是:

选项 | A | B | C | D |
X | C | Fe | Ca(OH)2溶液 | AlCl3 |
W | O2 | HNO3 | CO2 | NH3·H2O |
