题目内容
12.在单质的晶体中,一定不存在的粒子是( )| A. | 原子 | B. | 分子 | C. | 阳离子 | D. | 阴离子 |
分析 单质的晶体中一定不存在的微粒是阴离子,可能含有阳离子,由此分析解答.
解答 解:A、原子晶体中,晶体硅中中存在原子,故A正确;
B、稀有气体分子晶体中,只存在分子,故B正确;
C、单质的晶体中一定不存在的微粒是阴离子,可能含有阳离子,如金属晶体,故C正确;
D、在单质的晶体中,不可能存在阴离子,如有阴离子就不可能是单质,而是化合物,故D错误;
故选D.
点评 本题考查晶体的结构等知识点,此题可以用列举实例解题,试题培养了学生的分析能力及灵活应用能力,比较容易.

练习册系列答案
相关题目
20.在下列变化过程中,既有离子键被破坏又有共价键被破坏的是( )
| A. | 将 SO2通入水中 | B. | 烧碱溶于水 | C. | 将 HCl 通入水中 | D. | NaHSO4溶于水中 |
7.化学反应 A2+B2═2AB 的能量变化如图所示,则下列说法正确的是( )
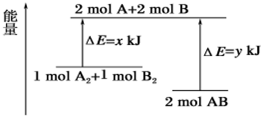

| A. | 该反应是吸热反应 | |
| B. | 断裂 1mol A-A 键和 1mol B-B 键能放出xkJ 的能量 | |
| C. | 断裂 2mol A-B 键需要吸收ykJ 的能量 | |
| D. | 2mol AB 的总能量高于 1 mol A2和 1mol B2的总能量 |
17.下列有关化学用语正确的是( )
| A. | 核内有 8 个中子的碳原子:68C | B. | 羰基硫(COS)的结构式: | ||
| C. | 乙烯的比例模型: | D. | NH4Br 的电子式: |
1.在室温时,下列各组中的物质分别与过量NaOH溶液反应,能生成5种盐的是( )
| A. | SiO2、N2O5、CO、Cl2 | B. | Al2O3、Cl2、N2O5、SO3 | ||
| C. | CO2、Al(OH)3、CaO、SO2 | D. | Al2O3、CO2、SO3、SO2 |
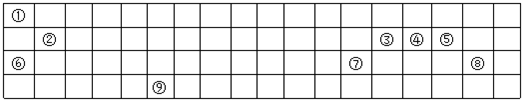
 ①~⑧是元素周期表中前四周期的8种元素,其相对位置如图所示.
①~⑧是元素周期表中前四周期的8种元素,其相对位置如图所示. .
.