题目内容
4.用元素符号或化学式回答原子序数11~17的元素的有关问题.(1)原子半径最小的元素是Cl;
(2)最高价氧化物对应水化物碱性最强的碱是NaOH;
(3)最高正价氧化物对应水化物酸性最强的酸是HClO4;
(4)写出(2)中的碱与(3)中的酸反应的离子方程式H++OH-=H2O;
(5)最高正价与负价绝对值相等的元素的氢化物是SiH4.
分析 从11到17号元素,这几种元素位于同一周期,同一周期元素,元素的金属性随着原子序数增大而减弱,元素非金属性随着原子序数增大而增强,
(1)除稀有气体外,同一周期元素中,原子半径随着原子序数增大而减小;
(2)同一周期元素,元素金属性越强,其最高价氧化物对应水化物碱性越强;
(3)同一周期元素,元素非金属性越强,其最高正价氧化物对应水化物酸性越强;
(4)强酸、强碱发生中和反应;
(5)第三周期最高正价与负价绝对值相等的元素是Si元素,位于第IVA族,其氢化物为硅烷.
解答 解:从11到17号元素,这几种元素位于同一周期,同一周期元素,元素的金属性随着原子序数增大而减弱,元素非金属性随着原子序数增大而增强,
(1)除稀有气体外,同一周期元素中,原子半径随着原子序数增大而减小,所以原子半径最大的是Na,原子半径最小的是Cl,故答案为:Cl;
(2)同一周期元素,元素金属性越强,其最高价氧化物对应水化物碱性越强,第三周期金属性最强的元素是Na,则碱性最强的是NaOH,故答案为:NaOH;
(3)同一周期元素,元素非金属性越强,其最高正价氧化物对应水化物酸性越强,第三周期非金属性最强的元素是Cl元素,则酸性最强的是HClO4,故答案为:HClO4;
(4)HClO4、NaOH都是强电解质,二者发生中和反应,离子方程式为H++OH-=H2O,故答案为:H++OH-=H2O;
(5)第三周期最高正价与负价绝对值相等的元素是Si元素,位于第IVA族,其氢化物为硅烷,化学式为SiH4,故答案为:SiH4.
点评 本题考查了同一周期元素周期律,明确同一周期元素金属性、非金属性及其相应化合物性质递变规律即可解答,熟练掌握元素周期律知识,灵活运用这些知识解答问题,题目难度不大.

练习册系列答案
相关题目
14.下列各组物质的晶体中,化学键类型完全相同、晶体类型也相同的是( )
| A. | CO2和SiO2 | B. | NaCl和HCl | C. | H2O和H2 | D. | KOH和KCl |
15.下列分散系中的分散质粒子大小属于纳米级(1-100nm)的是( )
| A. | Fe(OH)3胶体 | B. | Fe(OH)3沉淀 | C. | FeCl3溶液 | D. | 油水混合物 |
12.下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A. | 在0.1 mol•L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 在0.1 mol•L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) | |
| C. | 向0.2 mol•L-1NaHCO3溶液中加入等体积0.1 mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol•L-1]:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
13.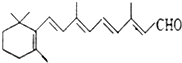 人们能够在昏暗的光线下看见物体,离不开视网膜中一种叫“视黄醛”的有机化合物,其结构简式如图所示,下列有关视黄醛的说法正确的是( )
人们能够在昏暗的光线下看见物体,离不开视网膜中一种叫“视黄醛”的有机化合物,其结构简式如图所示,下列有关视黄醛的说法正确的是( )
 人们能够在昏暗的光线下看见物体,离不开视网膜中一种叫“视黄醛”的有机化合物,其结构简式如图所示,下列有关视黄醛的说法正确的是( )
人们能够在昏暗的光线下看见物体,离不开视网膜中一种叫“视黄醛”的有机化合物,其结构简式如图所示,下列有关视黄醛的说法正确的是( )| A. | 视黄醛的分子式为C20H27O | |
| B. | 视黄醛可以使溴水和酸性高锰酸钾溶液褪色,也能发生银镜反应 | |
| C. | 视黄醛分子结构中含有苯环、碳碳双键和醛基 | |
| D. | 1mol视黄醛在催化剂的作用下最多可与5molH2发生加成反应 |
14.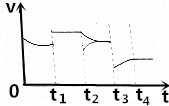 如图是反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的正反应速率随时间的变化图象,在t1时反应达到平衡状态,然后改变一个条件,v正的变化如图所示,则下列说法正确的是( )
如图是反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的正反应速率随时间的变化图象,在t1时反应达到平衡状态,然后改变一个条件,v正的变化如图所示,则下列说法正确的是( )
 如图是反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的正反应速率随时间的变化图象,在t1时反应达到平衡状态,然后改变一个条件,v正的变化如图所示,则下列说法正确的是( )
如图是反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的正反应速率随时间的变化图象,在t1时反应达到平衡状态,然后改变一个条件,v正的变化如图所示,则下列说法正确的是( )| A. | t1时改变的条件是增大压强,且平衡没有移动 | |
| B. | t2时改变的条件时减小甲醇的浓度,且平衡正向移动 | |
| C. | t2时改变的条件是增大了氢气的浓度,且平衡正向移动 | |
| D. | t3是改变的条件是升高温度,且平衡正向移动 |
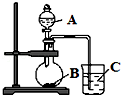 某研究性学习小组设计了一组实验,验证元素周期律.
某研究性学习小组设计了一组实验,验证元素周期律.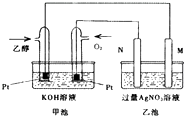 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题: