题目内容
某同学取等体积、等浓度的a.稀硫酸b.盐酸c.醋酸 三种酸溶液分别加入足量的铝粉进行反应,开始时三种溶液中反应速率快慢顺序是 ;(填字母,下同),反应完毕产生气体体积的大小顺序是 相同条件).
考点:化学反应速率的影响因素,弱电解质在水溶液中的电离平衡
专题:化学反应速率专题
分析:三种酸中,醋酸为一元弱酸,盐酸为一元强酸,硫酸为二元强酸,等浓度时,溶液中c(H+)大小顺序为a>b>c,c(H+)越大,反应速率越大,以此解答.
解答:
解:三种酸中,醋酸为一元弱酸,盐酸为一元强酸,硫酸为二元强酸,等浓度时,溶液中c(H+)大小顺序为a>b>c,c(H+)越大,反应速率越大,则开始时三种溶液中反应速率快慢顺序是a>b>c,完全反应,硫酸生成气体的体积最大,盐酸和醋酸相等.
故答案为:a>b>c;a>b=c.
故答案为:a>b>c;a>b=c.
点评:本题考查弱电解质的电离以及化学反应速率的影响因素,为高频考点,侧重于学生的分析能力的考查,注意把握弱电解质的电离特点,难度不大.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
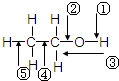 乙醇分子中各化学键如图所示,对乙醇在各种反应中断裂的键说明正确的是
乙醇分子中各化学键如图所示,对乙醇在各种反应中断裂的键说明正确的是( )
| A、和金属钠作用时,键②断裂 |
| B、和浓硫酸共热至170℃时,键①和⑤断裂 |
| C、和乙酸、浓硫酸共热时,键①断裂 |
| D、在铜催化下和氧气反应时,键①和②断裂 |
已知5KCl+KClO3+H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法正确的是( )
| A、KClO3是氧化剂,发生氧化反应 |
| B、氧化产物与还原产物质量比为5:1 |
| C、标准状况下,氯气的摩尔体积为22.4L |
| D、1mol KClO3参加反应时有10mol电子转移 |
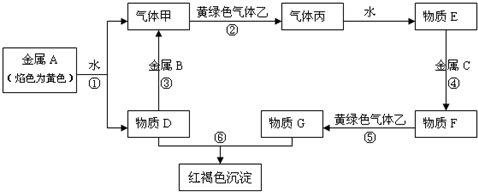
 A、B、C、D四种短周期元素,且A、D、B为相邻的同周期元素,C、B同主族,B、C可形成共价化合物BC3和BC2,A的原子结构示意图为如图,据此填空:
A、B、C、D四种短周期元素,且A、D、B为相邻的同周期元素,C、B同主族,B、C可形成共价化合物BC3和BC2,A的原子结构示意图为如图,据此填空: